V článku je uveden přehled aktuálních léčebných postupů u atopické dermatitidy dospělých. Pro objasnění souvislostí jsou nastíněny jak etiopatogeneze nemoci, tak i současná diagnostická kritéria. Základem sdělení je problematika lokální i celkové terapie.
Atopická dermatitida (AD) je chronické recidivující zánětlivé kožní onemocnění provázené úporným svěděním a suchostí kůže, podmíněné imunitní dysfunkcí a poruchou funkce kožní bariéry. Podobně jako bronchiální astma a alergická rinitida je součástí atopického (dermorespiračního) syndromu.
V rámci názvosloví se běžně setkáváme se zažitým pojmem ekzém, který v dermatologii používáme u projevů s alergickou etiologií. U nealergických projevů používáme termín dermatitida. V německy mluvícím prostředí i v českých zemích se používá označení ekzém, v anglosaském názvosloví atopická dermatitida – termín užívaný i u nás. V našem sdělení používáme proto oba pojmy. Setkat se můžeme i s dalšími analogickými názvy, jako neurodermitida, atopiformní dermatitida či endogenní ekzém.
Prevalence a klinické projevy onemocnění
Prevalence atopické dermatitidy se odhaduje u dětí na 10–20 % a u dospělých 3–5 % populace (obrázek 1).
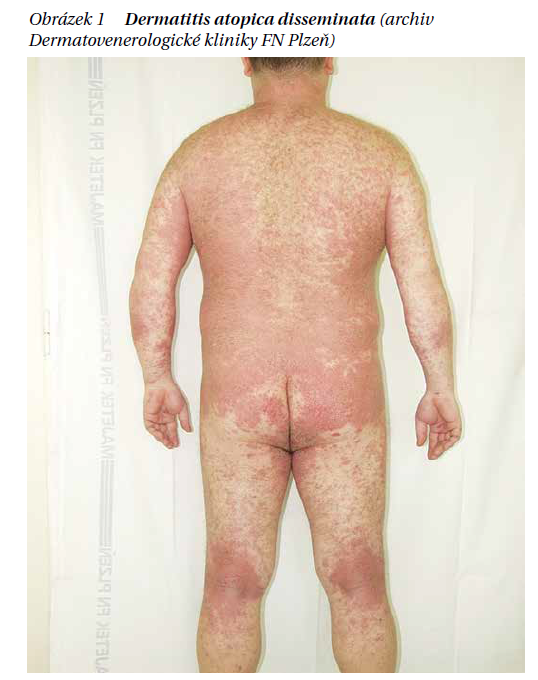
V průmyslových zemích se během posledních 40 let zvýšila trojnásobně. Tento nárůst AD má svou příčinu zejména ve změně životního stylu jedince i celé společnosti (tzv. hygienická teorie). Klinické projevy AD jsou pestré a individuálně velmi různorodé. Rozlišujeme formy flexurální (obrázek 2), nummulární, asteatotickou, dyshidrotickou, neurodermiformní, pruriginózní a erytrodermii.Společnými rysy pro všechny formy jsou chronický průběh, pruritus, xeróza a dermatitida. AD v dospělosti může být pokračováním klinických projevů z dětství, ale může se v tomto období objevit poprvé, a to s chroničtějším a závažnějším průběhem s poruchami spánku, snížením kvality života a psychosomatickými souvislostmi. Nepříznivými faktory jsou pozitivní rodinná anamnéza, časný vznik, těžší průběh AD v dětství a přítomnost respirační atopie.
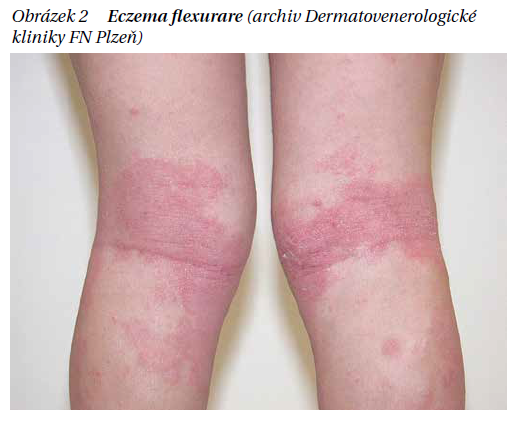
Etiologie a patogeneze
Rozlišují se dvě základní formy AD: alergická extrinzitní forma spojená s IgE zprostředkovanou senzibilizací a nealergická intrinzitní forma bez IgE zprostředkované senzibilizace představující 20–30 % pacientů. Obě formy jsou spojené s eozinofilií. V patogenezi AD hrají roli interakce mezi genetickými a environmentálními faktory, dysfunkcíkožní bariéry, mikrobiální nerovnováhou, imunitní dysregulací a environmentálními spouštěči zánětu kůže. Předpokládá se, že zánět je zahájen narušením epidermální bariéry s aktivací dendritických (Langerhansových) buněk, které interagují s Th2. Aktivované T buňky uvolňují do kůže cytokiny, zejména interleukin 4, interleukin 13 a interleukin 32, které aktivují následné cesty Janusovy kinázy(JAK). Cytokiny podporují zánět, svědění a produkci antigenu specifického IgE aktivací B buněk a plazmatických buněk.
Z genetických faktorů, které podporují dysfunkci kožní bariéry, jsou nejvýznamnější mutace v genu pro filaggrin (filament aggregating protein – FLG), který je produkován epidermálními keratinocyty rohové vrstvy. Je to protein významný pro tvorbu a posléze odlučování rohové vrstvy kůže. Mutace genů vede ke ztrátě funkce FLG a způsobuje narušení tvorby kožní bariéry a zvýšení transepidermální ztráty vody s následnou ichtyózou či folikulární hyperkeratózou. Vyšší aktivita enzymu sfingomyelin deacylázy u AD způsobuje změnu spektra ceramidů. Tyto intercelulární lipidy výrazně ovlivňují hydrataci, keratinizaci i imunologickou rovnováhu v kůži. Nedostatek kožních lipidů také snižuje produkci epidermálních antimikrobiálních peptidů, což vede k mikrobiální dysbióze. Toto narušení kožní bariéry navíc umožňuje aerogenním a potravinovým alergenům proniknout kůží a vyvolat senzibilizaci.
V predispozici a zhoršení AD hrají roli faktory prostředí (ty je třeba brát v úvahu i v rámci správného pracovního zařazení!). K nim patří extrémní teploty, expozice UV záření, znečištěné ovzduší (aktivací receptoru pro epidermální arylové uhlovodíky), zvýšená tvrdost vody a častější používání detergentů. Poslední z těchto faktorů souvisí s tzv. hygienickou hypotézou – důslednou sanitací sice dosáhneme snížení výskytu infekcí, ale současně tak vzrůstá počet alergických a autoimunitních onemocnění, včetně AD. Studie kožního mikrobiomu u pacientů s AD prokázala kolonizaci patogenním S. aureus. Tato změna mikrobiomu spolu se sníženou produkcí epidermálních antimikrobiálních peptidů je terénem pro následnou možnou impetiginizaci ekzému (obrázek 3).
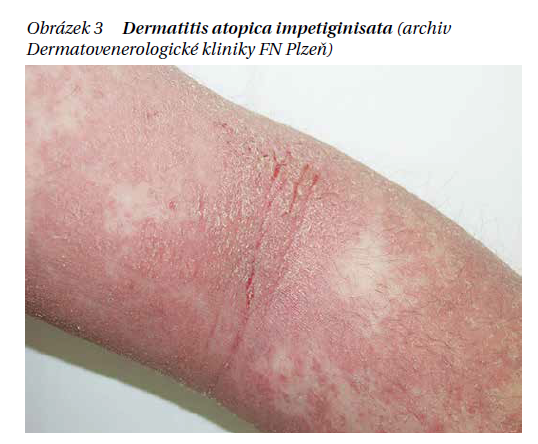
Pruritus u AD je založen na signalizaci mezi pruritogeny uvolňovanými keratinocyty, mastocyty a imunitními buňkami (T buňky a eozinofily) a malými senzoricko-nervovými vlákny v kůži. Pruritogeny zahrnují Th2 cytokiny (zejména IL-4, IL-14 a IL-31), tymický stromální lymfopoetin (TSLP) – prozánětlivý cytokin vznikající v keratinocytech u AD vedoucí k aktivaci Langerhansových buněk a stimulaci dalších zánětlivých buněk. K dalším pruritogenům patří histamin, proteázy a neuropeptidy. Tyto pruritogeny se vážou na receptory na senzorických C-nervových vláknech a A-delta nervových vláknech v epidermis a dermis a způsobují svědění a bolest. Pacienti s AD si, kromě svědění, často stěžují na bolestivé pocity, včetně pálení a píchání v oblastech ekzému. Většina pruritogenů se váže na nehistaminergní vlákna. Uvolňují se nejen zánětem, ale také škrábáním. To je hypotéza, která je v souladu s pocity pacientů, kteří uvádějí zintenzivnění svědění po škrábání (vztah k receptoru IL-4 alfa na nervových vláknech).
Diagnostika AD
Klinická diagnóza AD je založena na morfologických vlastnostech a distribuci kožních lézí, přítomnosti souvisejících klinických příznaků a charakteristické anamnéze. Diagnostická kritéria AD, která zpracovala Americká akademie dermatologie (AAD), jsou pro přehlednost uvedena v tabulce 1.
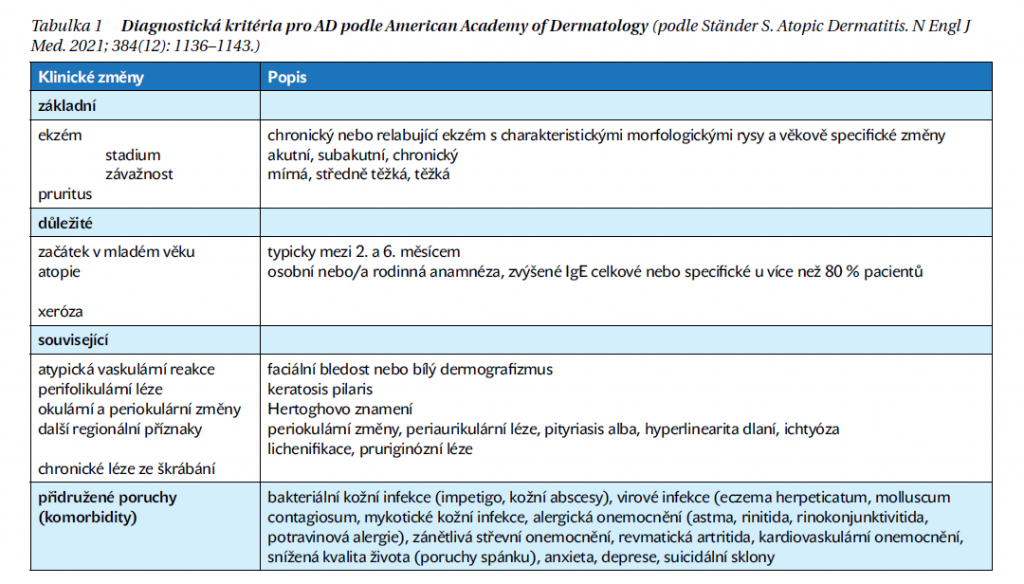
Závažnost AD lze kvantifikovat pomocí vícebodových skórovacích schémat, jako je oblast ekzému a index závažnosti (EASI) a stupnice skóre AD (SCORAD). Používají se v klinických studiích i v praxi. EASI hodnotí závažnost zarudnutí, tloušťky, exkoriace a lichenifikace a procento postižení kůže ve čtyřech oblastech (hlava, trup, paže a nohy). Skóre SCORAD zohledňuje více typů lézí a oblastí těla než skóre EASI a vypočítává se na základě oblasti postižené kůže a závažnosti zarudnutí, otoku, sekrece, tvorby krust, lichenifikace a xerózy, které se posuzují samostatně pro hlavu a krk, paže a DK, přední stranu trupu, záda a genitálie.
Terapeutické přístupy
Léčba AD musí probíhat v souladu s etiopatogenetickými hledisky a klinickou formou ekzému. Důležité je zjištění a eliminace všech zevních i vnitřních provokačních faktorů. Léčba AD spočívá v lokální aplikaci léčebných prostředků (případně léčbě fyzikální) a léčbě celkové.
Atopická dermatitida se dělí na tři skupiny závažnosti: mírnou, středně těžkou a těžkou. Mírná a středně těžká AD by měly být dobře zvládnutelné léčbou lokální, středně těžká až těžká AD vyžadují i léčbu celkovou.Odhaduje se, že těžkou AD trpí celkově cca 10 % pacientů, u dospělých ekzematiků se středně těžká až těžká AD vyskytují až u třetiny z nich. Evropské doporučené postupy rozlišují čtyři stupně léčby, kde se volba léčby odvíjí podle závažnosti průběhu (tabulka 2).
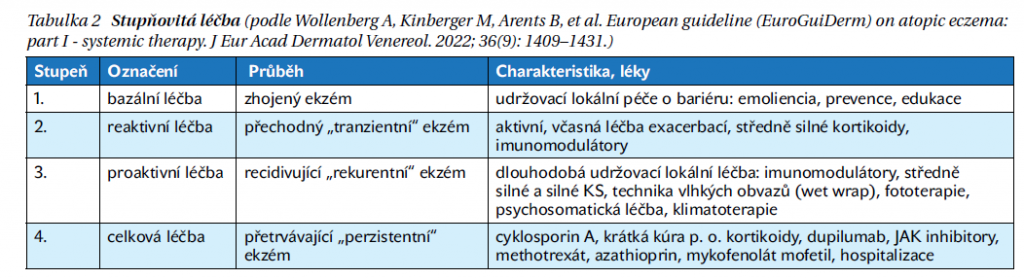
Lokální léčba
Lokální (topická) léčba je v dermatologii základem terapeutických postupů. Volba správné aplikační formy externa je v mnoha případech zásadní a je třeba jí věnovat pozornost!
U akutního ekzému i exacerbací chronického ekzému se aplikují místní léky(externa) ve formě vysychavých obkladů, pěn, lotionů, tekutých pudrů, chladivých past, krémů typu o/v i polyakrylátových nebo hydroxyetylcelulózových gelů. U subakutních forem jsou vhodné měkké pasty a krémy (typu o/v i typu v/o), na ochlupená místa roztoky, lotiony a gely. U chronického ekzému se používají mastné a řidší pasty, krémy typu v/o a masti. Na ochlupená místa lze aplikovat omyvatelné krémy a masti i speciální tinktury a gely. Použití léků ukazuje tabulka 3.
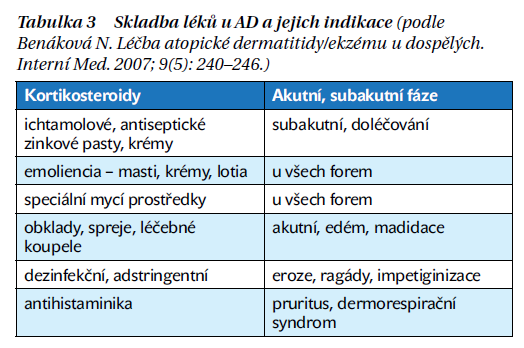
Základní léky k léčbě ekzému jsou kortikosteroidy. V akutní fázi onemocnění účinkují antiflogisticky, antiexsudativně, antialergicky a antipruriginózně, u chronického ekzému též antiproliferačně. Používají se ve formě mastí, krémů, gelů a lotionů. Dělí se na čtyři skupiny/třídy podle stupně účinnosti (tabulka 4).
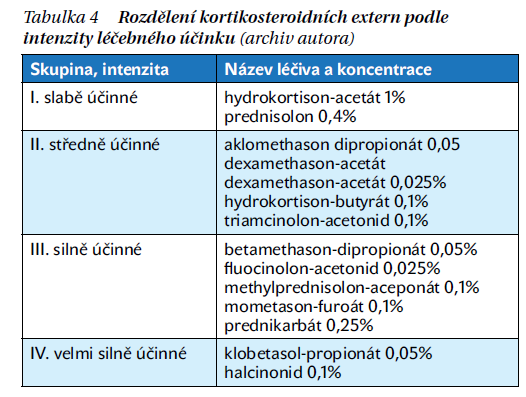
Kortikosteroidní externa lze kombinovat s dalšími látkami, a to s přihlédnutím ke konkrétní formě ekzémového postižení. U impetiginizace jsou to antibiotika (gentamycin, neomycin, kyselina fusidová), antiseptika (chloroxin, karbethopendecinum-bromid, chlorhexidin, klinochinol), v intertriginózních lokalizacích je možná kombinace s antimykotikem (klotrimazol). U chronických hyperkeratotických forem se aplikují v kombinaci s keratolytikem (kyselina salicylová). V rámci v dermatologii stále široce používané magistraliter receptury jsou další možnosti kombinací léčebných substancí, a to nejen s kortikosteroidy.
Pro použití lokálních kortikosteroidů jsou významná následující léčebná schémata:
- Ústupová léčba – po nástupu efektu co nejdříve snižujeme frekvenci aplikací (ob den, ob 2 dny… až po nejnižší ekzém zvládající interval).
- Sestupná léčba – po nástupu účinku přecházíme na slabší kortikoid (tabulka 3) a léčbu ukončujeme postupně, čímž eliminujeme riziko rebound fenoménu– zhoršení ekzému po rychlém přerušení léčby. Tento nežádoucí jev bývá poměrně častou chybou při nedostatečné edukacipacienta, která je neodmyslitelnou součástí léčby (nejen) topickými kortikosteroidy! Obecně by léčba topickými kortikosteroidy (TCs) měla být co nejintenzivnější a trvat co nejkratší dobu. Léčbu zahajujeme vždy silnějším kortikosteroidem.
- Intervalová léčba – při chronickém průběhu ekzému, kdy nelze stav v kratším časovém horizontu stabilizovat, přecházíme na interval aplikací 2× týdně (ob 3 dny). Tento způsob léčby snižuje možnost tachyfylaxe – navozené rezistence na kortikosteroid, kdy přímo úměrně s dobou aplikace klesá účinnost léku. Děje se tak při soustavné aplikaci kostikosteroidů, zpravidla více než dva týdny.
Rebound fenomén a tachyfylaxe jsou projevy závislosti kůže na lokálních kortikosteroidech zvané TSA (topical steroid addiction), kam patří i syndrom červené kůže (red skin syndrom – RSS), který se projevuje zarudnutím kůže po vysazení léčby, způsobeným vazodilatací kapilár.
Další léčebnou možností jsou lokální imunomodulátory (TIM). Jsou to inhibitory kalcineurinu pimekrolimus a takrolimus.Mají protizánětlivé účinky na úrovni slabě až středně silných kortikosteroidů, ale na rozdíl od nich jsou bez rizika tachyfylaxe, rebound fenoménu a nemají atrofogenní potenciál. Představují tak možnost relativně bezpečného ovlivnění dlouhodobého průběhu AD zejména v obličeji.
Fyzikální léčba – fototerapie, klimatoterapie a balneoterapie
Fototerapie je vhodným doplňkem léčby zejména u diseminovaných forem AD. Používá se UVB 311 nm s expozicí 2× týdně s dávkou od 0,2 J/cm2 do 1,5 J/cm2, UVA 2–3× týdně v dávce od 1,0 J/cm2 do 8 J/cm2 optimálně po dobu 2 měsíců ročně.
Součástí léčby AD je též balneoterapie, která může být realizována v návaznosti na hospitalizaci nebo jako její alternativa.
Celková léčba
Indikací celkové léčby jsou těžké refrakterní případy, kdy lokální léčba s případnou kombinací s fototerapií nevede k dostatečnému efektu nebo není tolerována. Cílem celkové léčby je u AD úleva od příznaků, reparace kožní bariéry a tlumení zánětu. Dále zvládnutí komorbidit a sekundárních komplikací, minimalizace nežádoucích účinků a maximalizace výsledku celkové léčby, včetně psychického stavu. Tedy stabilizace choroby až zhojení projevů.
V celkové léčbě AD jsou zásadními léky imunosupresiva. Tabulka 5 uvádí současný stav celkové léčby. K tomu je třeba dodat, že jediným registrovaným imunosupresivem k léčbě AD u dospělých v ČR i ve většině evropských zemí je cyklosporin A. Ostatní imunosupresiva se pohybují v kategorii „off label use“.
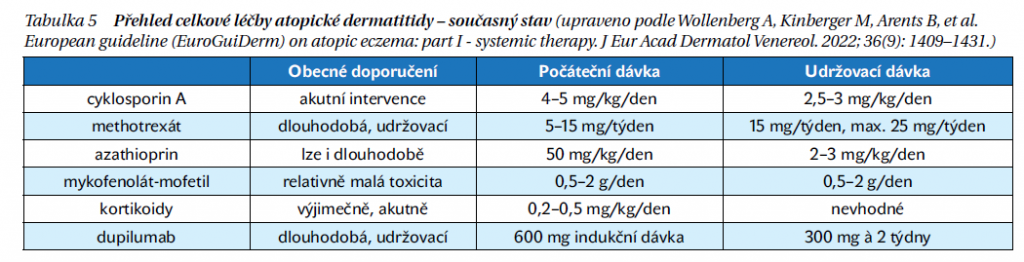
Cílená moderní léčba
Cílená moderní léčba je zcela novou skupinou v léčbě AD u pacientů, u kterých systémová konvenční léčba selže, není tolerována či je kontraindikována. V posledních letech došlo k obrovskému pokroku v popisu imunopatogenetických mechanizmů jejího vzniku a také v možnostech terapie. Je to především cílená terapie, kterou představuje biologická léčba a terapie malými molekulami, jejichž mechanizmus účinku spočívá v inhibici signální dráhy JAK/STAT. Prvním biologikem uváděným do praxe, v Evropě od roku 2017 a v ČR v roce 2018 registrovaným lékem, je dupilumab. Je to plně lidská monoklonální protilátka proti alfa řetězci receptoru pro IL-4 a IL-13. Působí nejen protizánětlivě, ale z výsledků studií vyplývá, že normalizuje i poruchy bariéry a mikrobiomu. Indikací je léčba středně těžké až těžké AD u dospělých, kteří jsou vhodnými kandidáty na systémovou terapii. Dupilumab patří v evropských doporučeních mezi léky první linie, který je v algoritmu volby celkového léku postaven na roveň cyklosporinu A. Preskripce v rámci příslušných kritérií je vázána na centra biologické léčby.
V oblasti malých molekul jsou k dispozici inhibitory Janusových kináz (JAK): abrocitinib (JAK1 inhibitor), baricitinib (JAK1, 2 inhibitor)a upadacitinib (JAK1 inhibitor).
Závěr
Atopická dermatitida je multifaktoriální onemocnění, jehož základem je porucha kožní bariéry s imunologickou dysbalancí včetně odchylek v rámci nespecifické imunity. Tyto dysfunkce jsou, spolu s genetickou predispozicí, navzájem úzce propojené a fenotypicky se projevují různými klinickými formami.
Základem léčby AD je léčba lokální, která musí být, vzhledem ke chronicitě onemocnění, soustavná, včas zahájená, účinná a odpovídat různým stupňům postižení kůže i rozmanitým klinickým obrazům. Ke zvládnutí středně těžkých až těžkých forem AD je zpravidla nutné přistoupit k léčbě celkové, která musí být v souladu s minimalizací nežádoucích účinků a maximalizací výsledného efektu.
Atopická dermatitida je obtížným problémem pro pacienta i lékaře. Profesionální přístup lékaře k pacientovi musí přispívat k vytvoření atmosféry důvěry, která je zásadní pro compliance. Všechny úrovně léčby AD mají svůj význam. Péče o kůži emoliencii, správné používání lokálních kortikosteroidů a imunomodulátorů, prevence spouštěcích faktorů, včetně psychosomatických, jsou zásadní přístupy ke zvládnutí tohoto nepříjemného a v mnoha směrech limitujícího kožního onemocnění. Účinná celková a zejména cílená moderní léčba mají pak v dlouhodobém horizontu potenciál ovlivnit výraznějším způsobem průběh AD, a tím zlepšit kvalitu života člověka s touto nemocí.
MUDr. Martin Novák
Dermatovenerologická klinika LF UK a FN Plzeň
