Kontinuální monitorace hladiny glukózy (CGM) představuje v současnosti preferovaný způsob selfmonitoringu koncentrace glukózy u lidí s diabetem, obzvláště u lidí s diabetem 1. typu léčených inzulinem v intenzifikovaném režimu. CGM prokazatelně zlepšuje úroveň glykemické kompenzace a má také příznivý efekt na snížení rizika hypoglykemie a zlepšení kvality života. V článku diskutujeme fyziologii regulace glykemie ve zdraví a při diabetu, technologii CGM – výhody, způsob vyhodnocování, limitace a její roli při edukaci pacienta a představujeme novou generaci CGM senzorů od firmy Dexcom – systém Dexcom G7.
Diabetes mellitus je polymorfní skupina onemocnění charakterizovaných mimo jiné hlavně poruchou regulace koncentrace glukózy v krvi. Na vzniku tohoto onemocnění se podílí několik známých patogenetických mechanizmů, a proto jednotlivé formy vyžadují odlišné přístupy k léčbě, aby byla účinná, ekonomicky přijatelná a nepříliš zatěžující pro pacienta. V našem přehledu se věnujeme významu kontinuální monitorace koncentrace glukózy pro léčbu diabetes mellitus 1. typu (DM1). Oblíbenou charakteristikou moderního přístupu k léčbě tohoto typu diabetu je: „Naším terapeutickým cílem je kromě jiného maximální možné napodobení fyziologické sekrece inzulinu.“ Je tedy třeba mít v první řadě jasno v tom, co se vlastně snažíme napodobit.
CO se snažíme napodobit?
Variabilita fyziologické koncentrace glukózy v krvi je poměrně úzká a tradičně udávaná v rozmezí 3,5–5,2 mmol/l na lačno, s posunem horní hranice na maximálně 11 mmol/l post-prandiálně. Této koncentraci odpovídá množství glukózy cca 1g na litr krve, tedy cca 4–6 g celkově. Při mírném zjednodušení to znamená, že při izokalorické diabetické dietě (200 g sacharidů/den) musí být během dne do krve vstřebáno cca 40× víc glukózy, kterou je nutné průběžně z krve distribuovat k utilizaci na energetické substráty či k uložení do zásob. Během noci (období lačnění) pak následuje mobilizace ze zásob tak, aby byla zachována dostupnost glukózy pro všechny buňky, které ji používají jako výhradní nebo téměř výhradní zdroj energie (mozek spotřebuje až 150 g glukózy za 24 hodin). Znamená to, že krví musí „projít“ velké množství glukózy při minimálních změnách její koncentrace a zanedbatelné pufrovací kapacitě krve pro glukózu. To předpokládá mimořádně účinný a přesný mechanizmus regulace, který je poskytován zdravými beta buňkami pankreatických ostrůvků ve spolupráci s inzulin senzitivními tkáněmi (tuk, sval, játra).
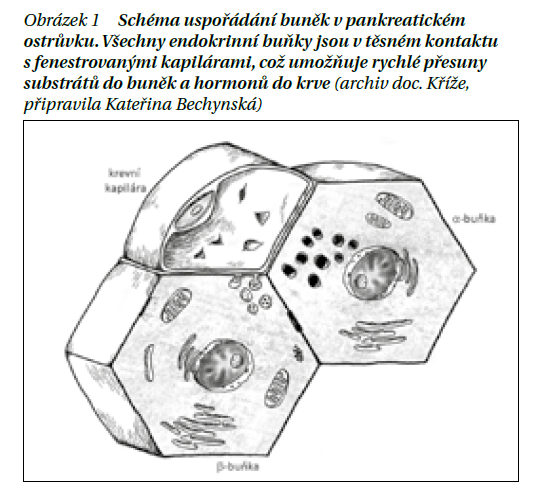
Beta buňky pankreatických ostrůvků jsou díky přímému kontaktu s fenestrovanými kapilárami v ostrůvcích „informovány“ o změnách koncentrace glukózy prakticky okamžitě (v řádu vteřin) a mohou opakovaně vyplavovat adekvátní mikro množství inzulinu přímo do krve kapilár pankreatu (obrázek 1). Mimořádně bohaté prokrvení pankreatických ostrůvků (představují 1 % objemu tkáně pankreatu, protéká jimi cca 20 % krve pro pankreas) umožňuje prakticky okamžitou distribuci inzulinu do portální žíly jater. Díky specifickému uspořádání endokrinních buněk v ostrůvcích tento systém umožňuje parakrinní inhibici alfa buněk inzulinem, který je lokálně cca 1 000× koncentrovanější než při aplikaci do podkoží. Alfa buňky tak jsou při vyšší glykemii plně inhibované a neuvolňují do krve žádný glukagon. Při poklesu glykemie se sekrece inzulinu zastaví, jeho koncentrace v ostrůvcích rychle klesne a alfa buňky mohou rychle reagovat vyplavením glukagonu. Současně je třeba zmínit, že polovina inzulinu přitékajícího do jater portální žilou se spotřebuje při prvním průchodu krve játry a nikdy se nedostane do systémového řečiště. Při poločase inzulinu 8–10 minut tak dochází při zastavení sekrece k velmi rychlému omezení jeho účinku na svaly a tuk. Tento mechanizmus umožňuje beta buňkám regulovat glykemii REAKTIVNĚ, tzn. reagovat změnou sekrece průběžně na změny koncentrace glukózy v tepenné krvi přitékající do pankreatu.
Jaké máme možnosti TO napodobit?
Vývoj technických prostředků pro měření koncentrace glukózy v tělních tekutinách, kvalita inzulinu a způsobů jeho aplikace je za 100 let od objevu způsobu získávání inzulinu naprosto ohromující. V porovnání se situací pacientů před 100 lety, kdy samotná aplikace zvířecího inzulinu prakticky naslepo (bez aktuální informace o glykemii) byla záchranou života, jsou dnešní možnosti kontinuální monitorace koncentrace glukózy v kombinaci s kontinuálním podáváním inzulinu v minidávkách skvělé. Nicméně hlavním limitujícím faktorem pro další zpřesňování a přibližování se přirozené (fyziologické) regulaci glykemie je místo, kde se koncentrace glukózy měří, a hlavně kam se podává inzulin – podkoží.
Nejmodernější v praxi používaná syntetická analoga inzulinu (ultra lispro) s nejlepší farmakokinetikou umožňují detekovat první molekuly inzulinu v krvi za 1–3 minuty po aplikaci do podkoží, cca za 10–15 minut je možné detekovat nástup biologického efektu (tj. zahájení utilizace glukózy) a teprve za 50–60 minut dosažení maximálního účinku. Na druhou stranu, i když nedojde k další aplikaci tohoto analoga, ještě za 4 hodiny doznívá jeho efekt a můžeme detekovat zbytková množství inzulinu v krvi.
Znamená to, že namísto série mikrodávek přímo do krve musíme do podkoží aplikovat celou dávku na období desítek minut. O velikosti dávky a načasování její aplikace je třeba uvažovat s předstihem a do rozhodování zahrnout kromě glykemického indexu a množství jídla i veškeré aktivity předcházející a bezprostředně následující aplikaci inzulinu, tedy rozhodovat PREDIKTIVNĚ. Pro reálnou možnost takového rozhodnutí máme k dispozici okamžitou a přesnou hodnotu glykemie změřenou v kapilární krvi, ale bez předchozí informace o trendu vývoje čili informaci neúplnou, a tedy nedostatečnou. Moderní alternativou je použití kontinuální monitorace koncentrace glukózy v intersticiální tekutině podkoží, která poskytuje informaci cca 10 minut starou, ale s kompletním průběhem za posledních několik hodin či dní. Tento přínos mnohonásobně převyšuje prodloužení nutné predikce o 10 minut.
Selfmonitoring glykemie při diabetu – historie a současnost
Není tomu až tak dávno (do začátku 80. let minulého století), kdy museli pacienti v domácím prostředí pravidelně vařit svou moč, aby mohli po přidání Benediktova činidla po několika minutách podle následné změny barvy stanovit přítomnost glukózy v moči. Prakticky to znamenalo, že získali informaci, je-li jejich glykemie vyšší než renální práh pro glukózu (10 mmol/l).
V 80. letech minulého století byly v USA do klinické praxe uvedeny kompaktní přístroje určené pro měření glykemie – glukometry. Samotný název glukometr byl převzat od komerčního názvu jednoho z prvních přístrojů tohoto typu – GLUCOMETER od firmy Bayer. Glukometry umožnily rychlé a poměrně přesné stanovení glykemie v reálném čase, nicméně v prvních letech byly dostupné pouze v ordinacích lékařů a teprve později bylo možné, aby je pacienti měli u sebe pro individuální potřebu. Zpočátku pro svou funkci potřebovaly velkou kapku krve, jejíž analýza trvala desítky vteřin. Do současnosti se významně zlepšila jejich spolehlivost, potřebný objem krve se snížil na malé desítky mikrolitrů a doba analýzy klesla na několik vteřin. Do praxe byly zavedeny tzv. glykemické profily – několik měření glykemie za den v přesně stanoveném čase vzhledem k příjmu potravy, které umožnily limitovaný náhled na fluktuaci glykemie v průběhu dne a noci.
Technologie CGM
Posledním velkým milníkem v selfmonitoringu glykemie byl příchod technologie CGM (continual glucose monitoring system) na přelomu tisíciletí. V roce 1999 byl v USA na trh uveden první GM systém MEDTRONIC MINIMED. Jednalo se o zaslepenou kontinuální nepřímou (neměří v krvi, ale intersticiální tekutině podkoží) monitoraci glykemie po dobu 3 dnů s nutností pravidelné kalibrace. Následoval senzor DEXCOM STS v roce 2006 a další. Prvním bezkalibračním CGM na trhu byl FREESTYLE LIBRE 1 od firmy ABBOTT, uvedený v roce 2017. Právě tento senzor byl doposud jediným představitelem tzv. intermittently scanned CGM (isCGM). CGM umožňuje kontinuální (většinou každých 5 minut) monitoraci hladiny glukózy v intersticiální tekutině bez nutnosti vpichů do prstů pacienta. Jedná se tak o kvalitativně (a i kvantitativně) odlišnou formu selfmonitoringu koncentrace glukózy, která vyžaduje nové způsoby vyhodnocování. V současnosti je standardem tzv. ambulatory glucose profile (AGP), ve kterém se vyhodnocuje 10 parametrů: počet dní hodnocení záznamu, procento času, kdy byl senzor aktivní, čas prožitý s koncentrací glukózy v jednom z 5 pásem (3,9–10 mmol/l, tzv. time in range [TIR], 2 pásma hypoglykemie a 2 pásma hyperglykemie), glykemická variabilita, průměrná glykemie a indikátor managementu glukózy (odhadovaný HbA1c). Mezi limitace CGM technologie patří alergické kožní reakce v místě aplikace CGM, dále zpoždění naměřené koncentrace glukózy v podkoží vůči glykemii o přibližně 5–15 minut (může hrát roli při rychle se měnící hladině glykemie a nástupu hypoglykemie), příliš častá korekce glykemie pacientem vyplývající z „nadbytku“ informací, který může vést až k úzkostným stavům.
DEXCOM G7
DEXCOM G7 byl na český trh uveden 1. prosince 2023. Jedná se o desetidenní senzor bez nutnosti kalibrace (tato možnost ale zůstala zachována) s možností otevřené i zaslepené monitorace. DEXCOM G7 je velmi přesný CGM senzor s hodnotami MARD 8,2 % na paži, která je optimálním místem aplikace, resp. 9,1 % na břiše. Systém si zachoval všechny výhody svého předchůdce a v několika podstatných aspektech došlo k dalším vylepšením. Autor textu, sám předchozí uživatel systému DEXCOM G6, podrobil systém DEXCOM G7 důkladnému testu, který mimo jiné zahrnoval několikahodinový pobyt v termálních lázních, několik pobytů v sauně a pravidelné sportovní aktivity. Senzor po celou dobu deklarované životnosti zůstal (i s pomocí náplasti, která je součásti balení) spolehlivě fixovaný na svém místě a byl funkční. Velikou výhodou oproti předchozí generaci je integrace vysílače a senzoru do jednoho zařízení a jeho podstatně nižší hmotnost a rozměry (obrázek 2). Zavádění senzoru pomocí aplikátoru bylo bezproblémové (obrázek 3). Další výhodou oproti DEXCOM G6 je výrazně zkrácená doba zahřívaní z předchozích 2 hodin na maximálně 30 minut a také dodatečných 12 hodin životnosti senzoru, která tak poskytuje uživateli více času na jeho výměnu. V tomto období je již možné zavést nový senzor a pro uživatele tedy nenastane situace, že nemá k dispozici CGM data po dobu zahřívání senzoru, jak tomu bylo v minulosti.


Senzor komunikuje s nově navrženou aplikací DEXCOM G7 (je potřebný „upgrade“ z aplikace DEXCOM G6), která má již v sobě integrován software na zpracování a vyhodnocení CGM dat DEXCOM CLARITY. Alternativou je použití přijímače (čtečky), tady však zůstává nutnost transferu dat do DEXCOM CLARITY pomocí USB kabelu. Velmi praktická je možnost blokace opakovaného alarmu při hyperglykemii. Když byl uživatel již jednou o hyperglykemii informován, resp. již aplikoval korekční dávku inzulinu, nechce být v následujících minutách opakovanými alarmy rušen. Začátkem roku 2024 v době uzavírky úpravy tohoto přehledu již byla realitou integrace DEXCOM G7 s hybridním uzavřeným okruhem Tandem Control IQ.
CGM další využití
Benefitem senzoru Dexcom G7 je možnost sdílení dat pomocí aplikace DEXCOM FOLLOW až s 10 osobami (předešlé verze Dexcom G6 s 5 osobami). Data sdílejí rodiče diabetických dětí nebo blízké osoby diabetiků, kteří žijí sami nebo mají zhoršené vnímání hypoglykemie. Je výhodou, že Dexcom upozorní až 20 minut před dosažením nízké glykemie, a je tedy dost času na řešení nejen při sportu nebo řízení motorového vozidla. Data z tohoto senzoru lze pomocí aplikace DEXCOM CLARITY sdílet se zdravotnickým zařízením, nebo data za určité období (obvykle za 30 dní) poslat ošetřujícímu lékaři. Data hodnotí lékař nebo edukační sestra spolu s pacientem, což má motivační efekt a edukace je vedena cíleně.
CGM se osvědčil i při redukci váhy. Jednak pacient vidí v reálném čase glykemii po jídle a snáz může zhodnotit výběr potravin a množství jídla. Včasné zachycení klesajících glykemií činí redukci váhy bezpečnou a předchází vzniku hypoglykemií, které jsou pro i tak obtížné motivování obézních pacientů velmi nevýhodné. U těhotných diabetiček, kdy je zapotřebí těsnější kompenzace, má CGM velký přínos, lze nastavit užší rozmezí v cíli a těsnější rozmezí alarmů.
CGM se stále častěji využívá při hospitalizaci pacientů léčených inzulinem, zdravotnický personál má snadnou a rychlou informaci o hladině glykemie. CGM se ponechává i při většině operací. Při některých vyšetřeních, jako magnetická rezonance nebo rentgen, se však musí senzor sejmout.
Podpořeno projektem Národní institut pro výzkum metabolických a kardiovaskulárních onemocnění (Program EXCELES, ID: LX22NPO5104) – Financováno Evropskou unií – Next Generation EU.
Podpořeno MZ ČR – RVO („Institut klinické a experimentální medicíny – IKEM, IČ 00023001“)
MUDr. Peter Novodvorský, Ph.D., MRCP
Bc. Vladimíra Havlová
Kateřina Bechynská
doc. MUDr. Jan Kříž, Ph.D.
Centrum diabetologie, IKEM, Praha
