Zhoubný novotvar prostaty je řazen do skupiny civilizačních chorob. Spolu s karcinomem prsu u žen patří k tzv. hormonálně senzitivním nádorům. Přestože zhoubné nádory prostaty nebývají agresivní a lze je dobře léčit, zemře na ně každý pátý muž. Dáno je to především pozdním odhalením nemoci. Terapie by měla být doporučena multidisciplinárním týmem. K léčebným modalitám patří obecně radioterapie, chirurgická léčba, hormonální terapie a chemoterapie. U vybraných nemocných může být zvolen přístup aktivního sledování nebo pečlivého vyčkávání.
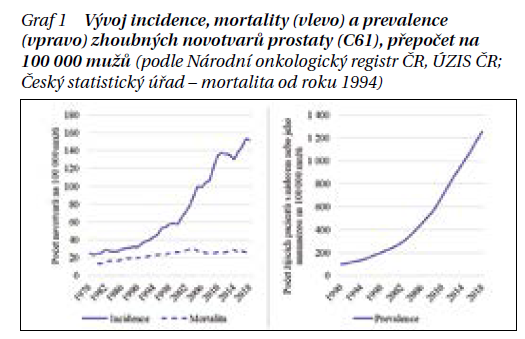
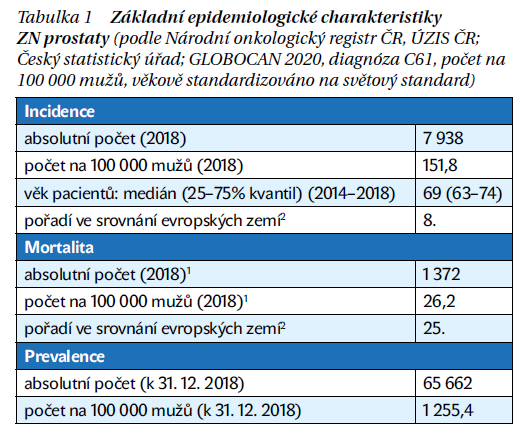
Incidence a prevalence zhoubných nádorů (ZN) prostaty v dlouhodobém trendu výrazně narůstá (graf 1). V roce 2018 bylo toto onemocnění nejčastěji diagnostikovaným novotvarem v ČR u mužů, kromě nemelanomových kožních nádorů. V roce 2018 bylo v ČR nově diagnostikováno celkem 7 938 případů, tedy 151,8 na 100 000 mužů. Při mezinárodním srovnání incidence stojí Česká republika v Evropě na 8. místě. Mortalita je v dlouhodobém časovém trendu stabilní, v Evropě obsazujeme 25. příčku. Věkovésložení nově hlášených ZN prostaty je 60–79 let. Z hlediska pokročilosti onemocnění bylo v období 2014–2018 70 % nově diagnostikovaných ZN prostaty zachyceno v klinickém stadiu I a II, což úzce souvisí s příznivou prognózou této diagnózy (tabulka 1).
Plánování léčby ZN prostaty vychází z preferencí informovaného pacienta. Podkladem k plánování terapie jsou výsledky histologie z biopsie prostaty, stadium nemoci, hladina PSA, Gleasonovo skóre. Roli hraje věk nemocného a jeho komorbidity.
ZN prostaty jsou na základě výše uvedených údajů rozděleny do hlavních skupin – lokalizovaný a lokálně pokročilý karcinom (nízce a vysoce rizikový), metastatický karcinom – mHSPC (hormonálně senzitivní) a CRPC (kastračně rezistentní).
U přibližně 5–10 % případů ZN prostaty se předpokládá familiární predispozice. Část těchto pacientů jsou nosiči germinálních mutací genu BRCA 1, 2 a téměř třetina pacientů má deficit v HRR genech (homologous recombination repair). Těmto nemocným můžeme nabídnout terapii PARP inhibitory.
Indikace ke genetickému vyšetření:
- ≥ 2 případy karcinomu prostaty u blízkých příbuzných, aspoň u jednoho ve věku ≤ 55 let;
- ≥ 3 případy karcinomu prostaty u blízkých příbuzných v jakémkoli věku;
- karcinom prostaty (Gleasonovo skóre ≥ 7, nebo primárně metastatický karcinom) a ≥ 1 případů karcinomu prostaty, prsu, ovaria nebo pankreatu u blízkých příbuzných.
Role PARP inhibitorů v terapii onemocnění
Inhibitory PARP blokují poly (ADP-ribóza) polymerázu (PARP) – enzym, který pomáhá opravovat poškozenou DNA. Proces spojování úseků DNA během kopírování je vysoce efektivní, ale není stoprocentní. Při přirozeném dělení buněk je potřeba opravit až desetitisíce nespojených, tzv. Okazakiho fragmentů (krátký polydeoxynukleotidový řetězec, který vzniká při replikaci na tom z vláken DNA, na kterém se replikační vidlice pohybuje ve směru 5–3, tzv. opožďující se řetězec).
Místa k opravě jsou rozpoznána enzymy z rodiny PARP. O těch je známo, že hrají významnou roli v jiném životně důležitém procesu, opravě zlomů vláken DNA vznikajících např. působením ionizujícího záření. PARP inhibitory brání spojování krátkých úseků DNA během kopírování DNA v buňce a meziprodukty nespojených Okazakiho fragmentů jsou pravděpodobně hlavním zdrojem cytotoxicity v rychle se dělících nádorových buňkách. Již delší dobu je protein PARP molekulárním cílem celé skupiny látek zvané PARP inhibitory, které se klinicky využívají pro léčbu karcinomů prsu, vaječníků a prostaty.
V ČR je ze skupiny PARP inhibitorů u ZN prostaty indikován olaparib.
Olaparib
Olaparib je účinným inhibitorem skupiny lidských enzymů poly (ADP-ribózo) polymerázy (PARP-1, PARP-2 a PARP-3) a byl prokázán jeho inhibiční účinek na růst určitých nádorových buněčných linií v prostředí in vitro a na růst nádoru v prostředí in vivo jak v monoterapii, tak v kombinaci se zavedenými metodami chemoterapie nebo novými hormonálními přípravky.
Terapeutické indikace:
- V monoterapii k léčbě dospělých pacientů s germinální a/nebo somatickou mutací BRCA1/2 metastazujícího kastračně rezistentního karcinomu prostaty (mCRPC), u kterých došlo k progresi po předchozí léčbě zahrnující nový hormonální léčivý přípravek. V léčbě olaparibem se doporučuje pokračovat do progrese onemocnění, nebo do nepřijatelné toxicity. U pacientů, kteří nejsou chirurgicky kastrovaní, má během léčby pokračovat léková kastrace analogem hormonu uvolňujícího luteinizační hormon (LHRH). Tato indikace se opírá o výsledky klinické studie PROfound, které byly publikovány v roce 2020. Hodnotila účinek olaparibu u pacientů s mCRPC po předchozí terapii ARTA.
- V kombinaci s abirateronem acetátem a prednisonem nebo prednisolonem k léčbě dospělých pacientů s mCRPC, u nichž není klinicky indikována chemoterapie. Doporučuje se pokračovat v léčbě do progrese nemoci, nebo do nepřijatelné toxicity. Léčba analogem hormonu uvolňujícího gonadotropin (GnRH) má během léčby pokračovat u všech pacientů nebo mají mít pacienti předchozí bilaterální orchiektomii.
Závěr
Terapie zhoubných nádorů prostaty zaznamenala v poslední době velký pokrok. Přes narůstající incidenci tohoto onemocnění je úmrtnost dlouhodobě přibližně stejná. Důvodem může být zavedení screeningového vyšetření. Díky němu je záchyt časných stadií I a II u 70 % mužů. ZN prostaty jsou u těchto nemocných vyléčitelné, nebo velmi dobře léčitelné. Dalším důvodem úspěchu je zavádění nových léčebných postupů a přístupů (ARTA, radikální operace v high volume centrech, rozšiřování možností radioterapie a zlepšování její techniky). Významnou roli hraje též zlepšování komunikace lékaře s pacientem. Informovaný pacient si tak může de facto vybrat léčebnou modalitu, kterou sám preferuje. Malé skupině nemocných s germinální nebo somatickou mutací BRCA1/2 a mCRCP lze nabídnout léčbu PARP inhibitorem v tabletové formě – olaparib, a to v monoterapii po přechozím selhání léčby novým hormonálním přípravkem, nebo v kombinaci s abirateronem acetátem a prednisonem u těch, u kterých není klinicky indikována chemoterapie.
MUDr. Hana Švébišová, Ph.D.
Oddělení klinické onkologie, Nemocnice Šumperk a.s.
