Trifluridin/tipiracil (FTD/TPI) je perorální kombinace thymidinového analoga trifluridinu a inhibitoru thymidinfosforylázy (TP) tipiracil hydrochloridu. Tipiracil inhibuje thymidinfosforylázu, enzym degradující trifluridin, udržuje přiměřenou koncentraci trifluridinu v plazmě, a tím potencuje jeho protinádorový účinek. Trifluridin je aktivní protinádorová komponenta, která je inkorporována do nádorové DNA. Kombinace FTD/TPI je schválena pro použití u pacientů s metastatickým kolorektálním karcinomem (mCRC), kteří jsou rezistentní ke standardní chemoterapii.
Účinek trifluridin/tipiracilu byl posuzován v četných klinických studiích. Mezinárodní multicentrická randomizovaná klinická studie fáze III RECOURSE hodnotila účinek trifluridin/tipiracilu ve srovnání s placebem v léčbě metastazujícího kolorektálního karcinomu refrakterního na předchozí chemoterapii. Studie RECOURSE prokázala významné zlepšení celkového přežití (OS) a doby do progrese (PFS) u pacientů léčených trifluridinem/tipiracilem. Medián OS byl 7,2 měsíce u pacientů léčených trifluridinem/tipiracilem ve srovnání s 5,2 měsíce u pacientů léčených placebem (HR = 0,69, p < 0,0001).
Popis případu
Třiapadesátiletá pacientka byla v roce 2011 vyšetřena kolonoskopicky pro pozitivní test na okultní krvácení. Vyšetřením byl zjištěn nádor v oblasti příčného tračníku, bez metastáz na CT.
Provedena byla resekce nádoru s histologickým nálezem invazivního adenokarcinomu grade 2 s fokální angioinvazí. Minoritně (10 %) byla popsána mucinózní komponenta, pět mízních uzlin bylo bez metastáz, tedy klasifikováno jako pT3 pN0 (uzliny[poz/vyš]: 0/5) L1. Nejednalo se o MSI-H nádor. Vzhledem k high risk II. klinickému stadiu (stenotizující nádor, mucinózní komponenta, lymfangioinvaze, nedostatečný počet vyšetřených lymfatických uzlin) byla indikována adjuvantní chemoterapie kapecitabinem. Léčba byla ukončena předčasně pro vznik stenokardií v souvislosti s chemoterapií.
Recidiva nádoru se objevila po třech letech v oblasti rekta s prorůstáním do děložního čípku. Solitární metastáza byla řešena operačně radikální abdominální hysterektomií, bilaterální adnexektomií a resekcí rekta. Histologie potvrdila infiltraci děložního čípku a stěny rekta tubulárním adenokarcinomem G2, morfologicky shodným s předchozím tumorem tračníku. Radioterapie nebyla indikována. Pooperačně byla podána chemoterapie režimem bolusový 5-FU (kontinuální 5-FU nebylo možné podat pro anamnézu stenokardií) v kombinaci s oxaliplatinou po dobu 6 měsíců. Dále byla pacientka sledována.
Druhá recidiva v malé pánvi se objevila po dalších dvou letech. Nález byl hodnocen jako resekabilní a následovala operace v rozsahu přední exenterace pánve, kolpektomie, s vytvořením ureteroileoanastomózy sec Bricker. Histologický nález prokázal v resekátu pochvy ložiskovou sekundární infiltraci tubulárním karcinomem kolorektálního typu. Radioterapie pooperačně nebyla indikována, chemoterapie rovněž ne (z důvodu předchozích nežádoucích účinků chemoterapie, neurotoxicitě po oxaliplatině, rozsahu a radikalitě operačního výkonu).
Po dalších třech letech klidu byla v rámci pravidelné kontroly zjištěna mírná elevace CEA. PET/CT zobrazilo ložisko ve zbytku pochvy a vícečetná ložiska metastáz v obou plicích (obrázek 1).
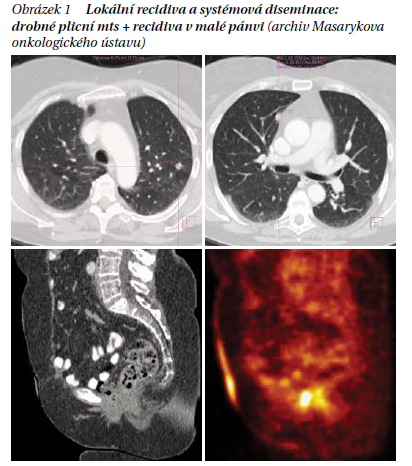
Doplnilo se prediktivní vyšetření RAS a BRAF. Nebyla zachycena mutace v genech KRAS, NRAS, BRAF. Pacientka zahájila systémovou léčbu 1. linie v kombinaci irinotekan a cetuximab. Tato léčba probíhala 7 měsíců s efektem stabilizace nemoci. Pro progresi plicních metastáz následovala 2. linie systémové léčby režimem bolusový 5-FU, leukovorin, oxaliplatina v kombinaci s bevacizumabem s efektem dlouhodobé stabilizace, PFS celkem 11 měsíců.
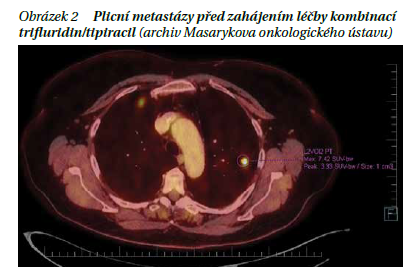
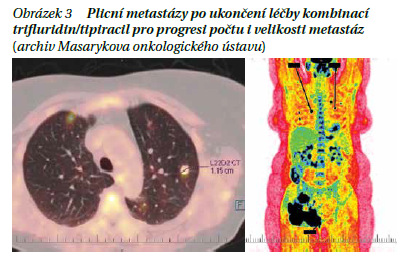
Pro progresi vícečetných bilobárních plicních metastáz i recidivy v oblasti poševního pahýlu (obrázek 2) byla zahájena 3. linie chemoterapie kombinací trifluridin/tipiracil. Celkově absolvovala 7 cyklů ve standardním dávkování 35 mg/m2 perorálně 2× denně 1.–5. den a 8.–12. den z 28denního léčebného cyklu. Nebyla nutná redukce dávkování. Pacientka zvládla léčbu bez projevů kardiotoxicity. Léčbou trifluridinem/tipiracilem byla dosažena dlouhodobá stabilizace nemoci. Z důvodu další progrese byla léčba kombinací trifluridin/tipiracil ukončena (obrázek 3). Vzhledem k výbornému výkonnostnímu stavu pacientky PS1 jsme nabídli pokračování v paliativní chemoterapii formou rechallenge irinotekanu s PFS 3 měsíců.
Závěr
Případ prokazuje příznivý léčebný účinek kombinace trifluridin/tipiracil u pacientky s mCRC v reálné praxi. Koreluje s výsledkem studie fáze 3b PRECONNECT, trifluridin/tipiracil zachovává u některých pacientů v reálné klinické praxi výkonnostní stav PS 0–1 v mediánu po dobu 8,7 měsíce.
Nejlepší mPFS byl dosažen u pacientů s dobrými prognostickými charakteristikami, tedy s nízkým nádorovým zatížením, bez jaterních metastáz a s méně agresivním onemocněním. Profil toxicity FTD/TPI a fluoropyrimidinu (5-FU) se liší. Na rozdíl od 5-FU je možné podat FTD/TPI i pacientům s deficitem dihydropyrimidin dehydrogenázy (DPD), protože TP je primární enzym, který metabolizuje trifluridine, a ne DPD.
Trifluridin/tipiracil má příznivý bezpečnostný profil a je zajímavým přípravkem nejenom v léčbě pacientů s mCRC.
MUDr. Beatrix Bencsiková, Ph.D.
Klinika komplexní onkologické péče, Masarykův onkologický ústav, Brno
