U karcinomu plic rozlišujeme dva základní typy, a to malobuněčný (small cell lung cancer – SCLC) a nemalobuněčný (non small cell lung cancer – NSCLC). Karcinom plic je v dnešní jedním z nejfrekventovanějších karcinomů na světě. Ročně na něj zemře více než 5 tisíc lidí. Jeho nemalobuněčná forma přitom postihne až 85 % z nich.
Biologická léčba, někdy také nazývaná cílená molekulová či terčová terapie, zasahuje vysoce selektivně do intracelulárních mechanizmů v dané nádorové buňce. Je určena pro nemocné s prokázanou řídicí mutací, na níž je daná molekula indikována. Nejčastěji se jedná o nízkomolekulární látky, které se váží například na receptory exprimované na povrchu nádorových buněk, a tím blokují signální dráhy vedoucí dál až do buněčného jádra. Takto jsme schopni ovlivňovat a znovu nastolovat nejzákladnější fyziologické regulační funkce buněk, mezi něž patří proliferace, diferenciace, migrace či angiogeneze.
I proto je velice důležité v rámci vyšetřovacího procesu nejprve detailně rozpoznat danou nádorovou tkáň. Včasné určení přesné morfologické klasifikace a daného podtypu (jako např. adenokarcinom či skvamózní karcinom) je pouze prvním krokem v rámci vyšetřovacího procesu. Vzhledem k dnešním možnostem imunoterapie a biologické léčby je tedy nezbytně nutné doplnit diagnózu o genetické testování na mutace. Standardně jsou dnes testovány EGFR, ALK, ROS1, ale je i mnoho dalších (tabulka 1).
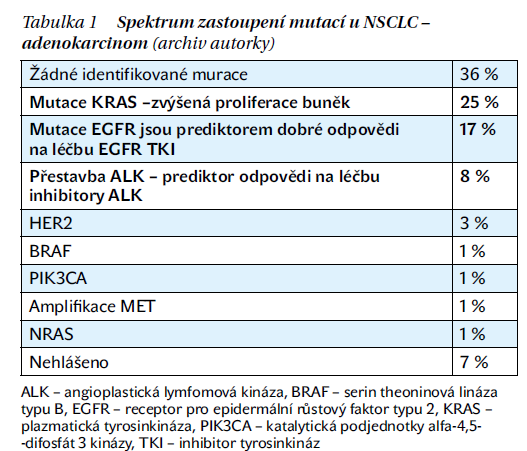
NSCLC je tudíž velice nehomogenní skupina, pacienti se stejným morfologickým typem mohou mít vysoce variabilní odpověď na stejný protinádorový preparát. Díky rychlému pokroku, obzvláště v oblasti technologie biologické detekce, jsme schopni preciznějšího a současně personalizovanějšího výběru terapie na základě zjištěných genetických změn.
Osimertinib a jeho mechanizmus účinku
Osimertinib se využívá u pacientů, v jejichž nádoru jsou prokázány tzv. aktivační mutace genu EGFR. Obecně můžeme říci, že vyšší výskyt mutací EGFR je v případě průkazu adenokarcinomu u nekuřáků, dále u žen a asijské populace.
Buněčný receptor EGFR/HER1 (epidermal growth factor receptor = receptor epidermálního růstového faktoru, humánní epidermální receptor, HER1) je povrchový receptor, který svou aktivitou zvyšuje tvorbu angiogenních faktorů, metastazování a zároveň blokuje fyziologický mechanismus apoptózy, takzvané buněčné smrti. Účinná látka osimertinib patří mezi inhibitory proteinových kináz. Přesněji se jedná o elektivní ireverzibilní inhibitor tyrosinkinázy EGFR 3. generace.
Přípravek Tagrisso je indikován v monoterapii v adjuvantní terapii po úplné resekci nádoru u dospělých pacientů s NSCLC, a to ve stadiu IB–IIIA, v případě, že se nádorová tkáň vyznačuje delecí na 19. exonu a bodovou mutací na 21. exonu (L858R). Tyto delece představují více než 90 % všech mutací genu EGFR. Dále je schválen u pacientů s pokročilým nebo metastazujícím NSCLC s aktivačními mutacemi EGFR a u nemocných s lokálně pokročilým nebo metastazujícím NSCLC s přítomnou mutací EGFR T790M.
Kazuistika
Naše kazuistika se zabývá 81letým pacientem bílé pleti, celoživotním nekuřákem. Pacient se chronicky léčil s arteriální hypertenzí, nevýznamnými chlopenními vadami a axiální hiátovou hernií s refluxní ezofagitidou.
Rodinná anamnéza
V rámci rodinné anamnézy jsme zjistili, že matka nemocného zemřela na rakovinu žaludku (83 let), sestra na rakovinu slinivky (74 let). Pacient v současné době pobírá starobní důchod, dříve pracoval jako projektant a konstruktér. V době prvozjištění nálezu pacient plně mobilní, orientovaný, samostatný, ECOG PS 0–1 (Eastern Cooperative Oncology Group Performance Status).
Na podzim 2021 utrpěl úraz v autobuse – naražená žebra na pravé straně. V té době byl indikován poúrazový rtg. snímek hrudníku, na němž byl popsán nález patologického stínu. Pacient proto absolvoval CT hrudníku s nálezem ložiska vzhledu primárního plicního tumoru a byl odeslán na naše pracoviště k dovyšetření.
Klinická vyšetření
První kontakt s pacientem proběhl na naší Klinice pneumologie Fakultní nemocnice Bulovka ke konci roku 2021. Po domluvě a se souhlasem pacienta jsme zahájili staginová vyšetření. Během tohoto vyšetřovacího procesu jsme doplnili PET CT, kde byl popsán hyperakumulující drobný tumor plic vlevo v dolním laloku anteromediálně bez průkazu postižení regionálních lymfatických uzlin a s absencí vzdálených metastáz. Vzhledem k možnosti chirurgického zákroku pacient absolvoval funkčí vyšetření (ventilační parametry i difuze zcela v normě) s rozhodnutím o schopnosti výkonu až do rozsahu pulmonektomie. Doplněna byla také bronchoskopie s BAL (bronchoalveolární laváž) v lokální anestezii, s cytologicky i mikrobiologicky negativním nálezem (obrázek 1 a 2).

Léčebné přístupy
Pro lokalizaci nádoru a zároveň absenci vzdálených metastáz jsme se rozhodli prezentovat pacientův případ na mezioborovém týmu, probíhajícím za účasti zástupců radiodiagnostického oddělení, chirurgické kliniky a v neposlední řadě kliniky pneumologie. V rámci multidisciplinárního jednání byl pacient indikován k VATS lobektomii (video-assisted thoracic surgery lobectomy) s peroperační biopsií. Ta byla provedena úspěšně a bez komplikací v lednu 2022.
Peroperačně byl histologicky identifikován adenokarcinom G2 s invazí do viscerální pleury a 2 lymfatických uzlin (reg 10L,7). Následně podle vyšetření mutací zjišťujeme negativitu PD-L1, ALK i ROS, avšak pozitivitu EGFR v exonu 21, další vzácné mutace NGS testování (next-generation sequencing) nebyly zachyceny. Zklamáním byl patologický staging pT2apN0, neboť na PET/CT nebylo pokročilejší stadium detekováno. Toto vyšetření proběhlo krátce před operací.
Vzhledem k vyššímu klinickému stadiu (IIIA) byla pacientovi na základě konzultace dalšího multidsciplinárního týmu, tentokrát pneumologicko onkologického, doporučena adjuvantní chemoterapie ve formě 2 cyklů a současně adjuvantní biologická terapie osimertinibem, ta však v té době byla podmíněna schválením přípravku Tagrisso revizním lékařem.
Necelý měsíc po operaci rozvinul nemocný paroxysmální fibrilaci síní s nutností farmakoverze.
Adjuvanci započal v březnu 2022 chemoterapií, a to v režimu karboplatina + vinorelbin, a ukončil o měsíc později, v dubnu. Během procesu se pacient cítil dobře, nebyl dušný, zvládal stále běžnou námahu. Po schválení úhrady přípravku Tagrisso, jsme zahájili v květnu konečně biologickou léčbu osimertinibem.
Terapie byla zahájena v denní dávce 80 mg. V červenci absolvoval nemocný CT hrudníku, kde trvá kompletní radiologická odpověď (obrázek 2). Vzhledem k negativnímu nálezu a výbornému klinickému stavu pacienta bylo vyžádáno další schválení adjuvantní léčby, tentokrát na 6 měsíců.
Pacient nyní nadále chodí na pravidelné kontroly CT hrudníku, jednou za 6 měsíců na průběžné rtg. hrudníku. Je bez známek lokální recidivy. V současné době je adjuvantní léčba již hrazena, a to na 3 roky. V případě našeho pacienta bude ukončena v dubnu roku 2025.
Závěr
Jak dokládají registrační studie na osimertinib v adjuvanci (ADAURA), i my jsme v praxi svědky tohoto malého zázraku. U nemocných s pozitivitou EGFR se významně snížila rekurence nemoci. Osimertinib je v této chvíli jediným z cílených léků v adjuvantním podání a my doufáme, že jen u něj nezůstane a i nemocní s ALK+, ROS1+ a další se dočkají podobné léčby.
Zároveň je třeba u léku vyzdvihnout i skvělou toleranci, čímž léčbu zvládnou i starší a „křehčí“ nemocní, jako je náš pacient.
MUDr. Adéla Komancová
Klinika pneumologie 3. LF UK a FN Bulovka
