Psoriatická artritida (PsA) je chronické zánětlivé onemocnění, charakterizované bolestí a ztrátou funkce periferních kloubů (artritida), postižením páteře (axiální spondylitida, sakroiliitida), entezitidou, daktylitidou, postižením kůže (psoriáza PsO) a nehtů, a proto je nazývána „psoriatickou nemocí“. Psoriatická artritida se řadí do skupiny spondyloartritid. Postižení orgánů asociovaných s PsA (psoriáza, uveitida a zánětlivé onemocnění střev) se nově nazývá „nemuskuloskeletální“ (non-musculoskeletal) manifestace, která nahrazuje termín „mimokloubní“ (extra-articular) manifestace.
Při výběru terapie je třeba vzít v úvahu komorbidity asociované s PsA (např. obezita, metabolický syndrom, nealkoholická steatóza jater, kardiovaskulární onemocnění a deprese). Výběr léku ovlivňuje klinická manifestace, aktivita onemocnění a také věk, preference pacienta, plánované rodičovství a potenciální nežádoucí účinky.
Časná diagnostika a léčba, navození remise nebo minimální aktivity onemocnění jsou dnešním základním cílem léčby. Pravidelně musíme hodnotit aktivitu onemocnění a upravit terapii podle strategie „léčba k cíli“ (treat to target). Do roka od nástupu příznaků dochází ke vzniku erozí u 27 % pacientů a 47 % má eroze do dvou let. Remise je možná až u 60 % pacientů s PsA. V dlouhodobém horizontu chceme zabránit strukturálnímu postižení. Negativní prediktivní faktory rozvoje kloubního poškození zahrnují polyartikulární postižení, zvýšené hladiny reaktantů akutní fáze, strukturální poškození – erozivního onemocnění kloubů, daktylitidu, postižení nehtů a průkaz nedostatečné odpovědi na počáteční terapii.
Optimální terapie zahrnuje nefarmakologické intervence, včetně edukace pacienta, fyzikální a pracovní terapii, rehabilitační cvičení, výživu, psychologické poradenství a ortopedickou chirurgii. Důležitá je spolupráce mezi revmatologem a dermatologem.
Farmakoterapie
Chorobu modifikující léky (DMARDs) dělíme na syntetické konvenční (csDMARDs – methotrexát, sulfasalazin, leflunomid), které představují možnost první volby u pacientů s aktivní psoriatickou artritidou (PsA) po selhání léčby nesteroidními antirevmatiky (NSAID) i u již zavedené PsA. Syntetické cílené léky (tsDMARDs – tofacitinib, upadacitinib, apremilast – inhitibor fosfodiesterázy 4 – PDE 4), které cíleně inhibují intracelulární signalizační kaskádu a biologické léky (bDMARDs anti-TNF a IL-17i, IL-12/23i) (tabulka 1, schéma 1).
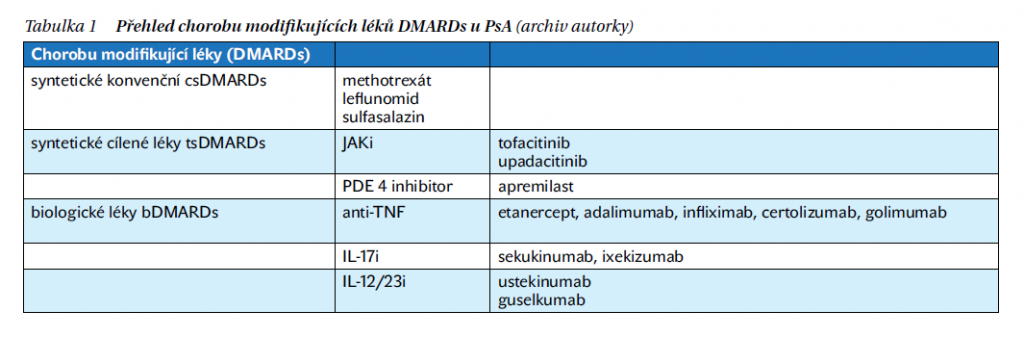
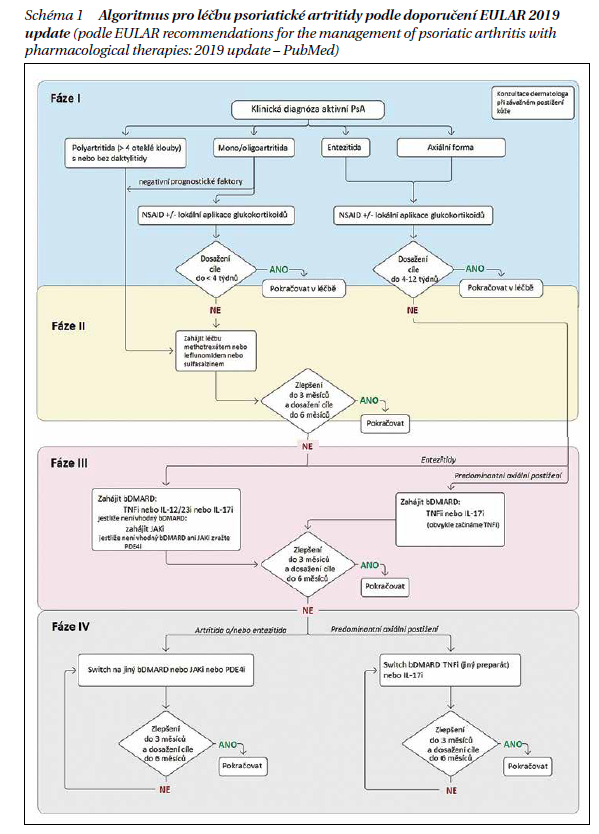
PsA byla dříve přirovnávána k mírné formě séronegativní revmatoidní artritidy (RA), nyní je však uznávána jako samostatná jednotka s jedinečnými klinickými příznaky. Vzhledem k tomu, že v minulosti byl zvažován podobný etiopatologický vztah s RA, byla terapie DMARDs pro léčbu PsA založena hlavně na důkazech původně odvozených z klinických studií RA. Obecně se u aktivní PsA doporučuje csDMARD methotrexát (MTX), leflunomid (LEF), sulfasalazin (SAS). Nejčastějšími nežádoucími účinky jsou infekce a gastrointestinální intolerance.
U tradičních chorobu modifikujících antirevmatických léků (csDMARD) nebylo prokázáno, že účinně léčí všechny klinické projevy psoriatického onemocnění (např. axiální symptomy, uveitidu, entezitidu a daktylitidu) ani neinhibují strukturální poškození periferních kloubů. Naproti tomu anti-TNF účinně léčí všechny domény aktivity onemocnění u PsA a bylo prokázáno, že zabraňuje progresi radiografického poškození.
Methotrexát je jedním z nejčastěji používaných systémových léků pro PsA užívaný jako „kotevní lék“. Vhodná dávka je 15–25 mg jednou týdně perorálně. Parenterální aplikace může pomoci zvýšit účinnost a snížit vedlejší účinky MTX. Pacienti dlouhodobě léčení MTX vyžadují pravidelné laboratorní monitorování krve à 3 měsíce (krevní obraz, jaterní enzymy a sérový kreatinin). Methotrexát má embryotoxické účinky, způsobuje potraty a fetální malformace, a proto je kontraindikován v těhotenství.
Leflunomid je účinnou a dobře tolerovanou možností pro PsA s příznivými účinky na periferní artritidu, bolest, únavu, daktylitidu a kožní postižení. Udržovací dávka je 20 mg denně. Monitorování leflunomidu je podobné jako u MTX. Není vhodný při plánovaném těhotenství, po ukončení léčby je nutné vyčkat až 2 roky.
Sulfasalazin byl u PsA studován nejrozsáhleji. SAS poskytuje určité zlepšení funkčního výsledku. S opatrností je možné užívání v graviditě v nejnižší možné dávce.
Biologická léčba
Tumor nekrotizující faktor α (TNFα) je prozánětlivý cytokin v imunopatogenezi psoriázy a PsA, jeho přítomnost byla prokázána v zánětlivé synovii, entezích a také v psoriatickém ložisku kůže. V současnosti je celosvětově schváleno pět inhibitorů tumor nekrotizujícího faktoru (anti-TNF) pro léčbu PsA: etanercept, infliximab, adalimumab, golimumab a certolizumab pegol, které jsou účinné a relativně bezpečné pro léčbu periferní artritidy, psoriázy a inhibují strukturální poškození. Infliximab a golimumab jsou účinné u daktylitidy a entezitidy.
Další cíle v léčbě PsA jsou v drahách IL-17 a IL-23. Signalizace IL-17 prostřednictvím jeho receptoru je unikátní, protože nevyužívá Janusovu kinázu (JAK) a aktivátor transkripce (STAT) dráhu; spíše se spojuje s adaptorovým proteinem ACT1, který následně aktivuje nukleární faktor κB (NF-κB). IL-17 zvyšuje expresi prozánětlivých cytokinů. Cílená terapie proti IL-17 až IL-23, klíčových cytokinů zapojených do dráhy aktivace lymfocytů Th 17 je účinná při léčbě psoriázy, psoriatické artritidy, entezitidy a daktylitidy.
IL-23 sdílí společnou podjednotku p40 s IL-12, a je proto blízce příbuzný. Aktivace této zánětlivé dráhy se podílí na všech čtyřech typických rysech PsA: zánět kůže a kloubů, erozivní kostní onemocnění a patologická novotvorba kosti.
Inhibitory TNFα (anti-TNF)
Inhibitory tumor nekrotizujícího faktoru (anti-TNF) mají jedinečnou výhodu účinnosti při léčbě axiálního postižení, entezitid a daktylitid, u kterých csDMARDs vykazují malý účinek. Na rozdíl od tradičních DMARDs bylo prokázáno, že anti-TNF inhibuje radiografickou progresi v periferních kloubech.
Indikace anti-TNF u periferní artritidy je při selhání léčby csDMARDs po 3–6 měsících (nedosažení minimální aktivity MDA nebo remise). V případě těžké daktylitidy (3 a více postižení prstů) a těžké entezitidy (3 a více míst) po selhání terapie NSA a 2 lokálních aplikací glukokortikoidů. U axiální formy je biologická léčba indikována při BASDAI > 4, bez předchozí terapie csDMARDs.
Etanercept (Enbrel, Erelzi, Benepali)
Etanercept je rozpustný receptorový fúzní protein, který se váže na solubilní TNFα, který antagonizuje. K léčbě PsA se etanercept podává s. c. v dávce 50 mg týdně, nebo alternativně 25 mg dvakrát týdně.
Infliximab (Remicade, Remsima, Inflectra, Flixabi, Zessly)
Infliximabje chimérická monoklonální protilátka TNFα, která se váže na solubilní i membránově vázaný TNFα a inhibuje ho. Komplex váže komplement a vede k lýze buňky. Infliximab neváže TNFβ. Molekula infliximabu je tvořena ze 75 % humánní a ze 25 % myší komponentou. V úvodu léčby se podává infuze i. v. v dávce 5 mg/kg (rozmezí 5–10 mg/kg), v intervalu 0, 2, 6 týdnů a následně každých 8 týdnů s možností kratších intervalů, pokud je to klinicky indikováno. Infliximab (Remsima) lze podávat i subkutánně (po 2 infuzích intravenózního infliximabu podaných v rozmezí 2 týdnů). Doporučená dávka přípravku Remsima k subkutánnímu podání je 120 mg jednou za 2 týdny. Methotrexát je vhodný i k omezení antichimérických protilátek (HACA).
Účinnost infliximabu, včetně zpomalení rentgenové progrese u PsA, byla prokázána ve studii IMPACT 1 a 2. Kromě kožních a kloubních projevů tato studie hodnotila také daktylitidu, entezitidy, funkční stav a kvalitu života.
.
Adalimumab (Humira, Hulio, Hyrimoz, Hukyndra, Idacio, Imraldi, Yuflima)
Adalimumabje rekombinantní lidská anti-TNFα monoklonální protilátka, která se váže na solubilní i membránově vázaný TNFα a inhibuje ho. K léčbě PsA se podává v dávce 40 mg s. c. každé 2 týdny.
Účinnost adalimumabu byla potvrzena ve studii ADEPT. Radiografická progrese onemocnění byla významně zpomalena. Jde o vhodný preparát při zánětlivém postižení střeva (IBD) nebo při recidivujících uveitidách.
Golimumab (Simponi)
Golimumab je plně humanizovaná monoklonální protilátka anti-TNFα, která se váže na solubilní i membránově vázaný TNFα a interferuje s jeho aktivitou, váže komplement a vede k lýze buňky. Podává se v dávce 50 mg s. c. každé 4 týdny. Na základě studie GO-REVEAL byl prokázán účinek i na entezitidy, daktylitidy, postižení kůže a nehtů a radiografickou progresi.
Certolizumab (Cimzia)
Certolizumab pegol je pegylovaný humanizovaný anti-TNFα antigen vázající fragment (Fab). Certolizumab neutralizuje solubilní i membránově vázaný TNFα. Na rozdíl od jiných monoklonálních protilátek TNFα postrádá Fc oblast, a proto neaktivuje cytotoxicitu závislou na protilátkách, zprostředkovanou buňkou nebo cytotoxicitu závislou na komplementu. Podává se v dávce 200 mg s. c. každé 2 týdny nebo alternativně 400 mg s. c. každé 4 týdny.
Studie RAPID-PsA prokázala účinnost certolizumabu u PsA. Zlepšení byla také pozorována s ohledem na onemocnění nehtů, entezitidy a daktylitidy, včetně radiologické progrese. Pacientky ho mohou s opatrností užívat celé těhotenství.
Bezpečnost a snášenlivost
Kromě své role u autoimunitního onemocnění hraje TNFα důležitou roli v obraně hostitele. V důsledku toho inhibice TNFα potenciálně zvyšuje riziko infekcí. Nicméně anti-TNF byly v klinických studiích dobře tolerovány, přičemž míra infekce byla jen mírně vyšší než u placeba. Nejčastěji hlášené nežádoucí účinky zahrnují infekce horních cest dýchacích, nazofaryngitidu a reakce v místě vpichu/infuzi.
Maligní onemocnění a závažné infekce jsou mnohem méně časté. Údaje z klinických registrů, které poskytují důkazy o dlouhodobé bezpečnosti anti-TNF než kratší klinické studie, neodhalily žádné zvýšené riziko solidních nádorů, ale mírně častější výskyt nemelanomových karcinomů kůže. Reaktivace tuberkulózy byla hlášena u všech anti-TNF, ale je extrémně vzácná. Riziko lze snížit screeningem před zahájením léčby (rentgenu hrudníku, vyšetření Quantiferron).
Celkově u PsA měl anti-TNF bezpečnostní profil obecně podobný tradičním DMARD, přičemž byl významně účinnější při léčbě všech domén aktivity onemocnění. Většina pacientů je dobře snáší.
Inhibitory IL-12/IL -23
Lepší pochopení patofyziologie PsA umožnilo novou éru v léčbě pacientů. Zacílení na dráhu IL-17 a osy IL-12–IL-23 poskytuje nový biologický cíl po anti-TNF léčbě.
Ustekinumab (Stelara)
Ustekinumab je plně humánní monoklonální protilátka IgG1k, která se váže na společnou podjednotku p40 cytokinů IL-12 a IL-23. IL-12 je klíčový cytokin v zánětlivé odpovědi Th1 a IL-23, který se účastní aktivace buněk Th17 k produkci IL-17. Aplikuje se 45 mg s. c., dále pak za 4 a každých 12 týdnů. Účinnost a bezpečnost ustekinumabu u pacientů s PsA byla stanovena ve studii PSUMMIT 1 a 2. Nebyl prokázán efekt na rentgenovou progresi.
Guselkumab (Tremfya)
Guselkumab je plně humánní monoklonální protilátka IgG1l s vysokou specificitou a afinitou a selektivně se váže na protein IL-23 proti IL-23-p19. Podává se 100 mg s. c. v nultém a 4. týdnu, následovaných udržovací dávkou každých 8 týdnů. Studie DISCOVER 1, 2 prokázala účinek na artritidy, entezitidy, daktylitidy a psoriázu. Bezpečnostní profil byl sledován ve studii Cosmos, kde nebyly zjištěny žádné případy malignity, IBD nebo deprese.
Inhibitory interleukinu 17
Sekukinumab (Cosentyx)
Sekukinumab je plně humánní monoklonální protilátka proti IL-17A, u které bylo prokázáno, že ve dvou dávkách funguje lépe než etanercept na psoriázu (PsO) v přímé studii FIXTURE. Sekukinumab je účinný u PsA podle studie FUTURE 1 a 2. Podává se v dávce 150 mg s. c., kterou lze navýšit na dávku 300 mg à 4 týdny. Bylo prokázáno zpomalení rentgenové progrese u PsA. Bezpečnostní profil souvisí s možným zvýšením rizika infekce horních dýchacích cest, nazofaryngitidy a kandidózy. Nebyly hlášeny žádné případy tuberkulózy.
Ixekizumab (Taltz)
Ixekizumab je rekombinantní humanizovaná monoklonální protilátka IL-17A. Zahájíme dávkou 160 mg s. c. (dvě injekce po 80 mg) v týdnu 0, následováno dávkou po 80 mg (jedna injekce) každé 4 týdny. Při léčbě inhibitory IL-17 byly hlášeny nové případy nebo exacerbace zánětlivého střevního onemocnění, proto se nedoporučuje pro pacienty se zánětlivým střevním onemocněním.
Inhibitor fosfodiesterázy 4 (PDE4)
PDE4 je nejspecifičtější izoforma enzymu hydrolyzujícího cAMP, má čtyři různé izotypy (A, B, C a D) a více než 20 různých izoforem. Primárně je exprimován v imunitních buňkách a v buněčných typech zapojených do patogeneze psoriázy a psoriatické artritidy, jako jsou keratinocyty, endoteliální buňky a synoviální buňky, což z něj činí atraktivní terapeutický cíl.
Apremilast (Otezla) (
Apremilast je malá molekula (s molekulovou hmotností nižší než 1 kDa), která specificky inhibuje PDE4, aniž by vykazovala selektivitu mezi izotypy PDE4, což vede ke zvýšení cAMP a následné aktivaci proteinkinázy A s následným snížením TNF, IL-12 a IL-23. Biologicky jsou dobře dostupné ze střeva, a proto jsou podávány perorálně. Účinnost byla prokázána ve studii PALACE I, II a III. Mezi nejčastější nežádoucí patřily průjem, nauzea a nazofaryngitida.
Inhibitory JAK
Rodina JAK (Janusovy kinázy) má čtyři členy (JAK1, JAK2, JAK3 a tyrosin-proteinkinázu 2 (TYK-2). JAK jsou cytoplazmatické tyrosinkinázy, které mají dvě domény přenášející fosfát, jednu s kinázovou aktivitou a druhou, která negativně reguluje první. Hrají zásadní roli v signální transdukci různých cytokinů. Aktivované receptory rekrutují JAK a následně se autofosforylují. To umožňuje vazbu členů rodiny signálních přenašečů a aktivátorů transkripce (STAT), které jsou také fosforylovány JAK.
Tofacitinib (Xeljanz)
Tofacitinibje inhibitor signální dráhy JAK-STAT, inhibitor JAK3 a JAK1 a v menší míře i JAK2, schválený pro léčbu RA. Tofacitinib prokázal účinnost u pacientů se středně těžkým až těžkým PsO nebo PsA (OPT Pivotal 1 a OPT Pivotal 2). Tofacitinib je také indikován u pacientů se středně těžkou a těžkou formou ulcerózní kolitidy. Podává se perorálně 5 mg dvakrát denně. Opatrnost je namístě u pacientů starších 65 let vzhledem ke zvýšenému riziku závažných infekcí (leukopenie), infarktu myokardu (hyperlipidemie) a malignit.
Upadacitinib (Rinvoq)
Upadacitinib je selektivní a reverzibilní inhibitor Janusovy kinázy (JAK). V lidských buněčných testech upadacitinib přednostně inhibuje signalizaci pomocí JAK1. Upadacitinib je indikován u PsA, AS a ulcerózní kolitidy. Podává se perorálně 15 mg jednou denně.
Závěr
Klinické důkazy ukazují, že cílená léčba proti TNFα je účinnou terapeutickou strategií při léčbě PsA. Všech pět anti-TNF preparátů prokázalo významnou účinnost při léčbě PsA, stejně jako inhibici radiografické progrese. Jsou to bezpečné a účinné léky, které způsobily revoluci v přístupu k léčbě PsA, zlepšení kvality života a funkčního stavu. Dnes se již staly zlatým standardem pro léčbu PsA.
Ne všichni pacienti jsou však schopni dosáhnout nebo udržet nízkou aktivitu onemocnění. Určité procento pacientů na anti-TNF terapii nereaguje (primární selhání léčby). Někteří pacienti mají kontraindikace k užívání anti-TNF, nesnášenlivost nebo závažné nežádoucí účinky. Nové biologické léky s jiným mechanizmem účinku inhibují IL-12/23 (ustekinumab), IL-17 (sekukinumab, ixekizumab), IL-23 (guselkumab, tildrikizumab, risankizumab), abatacept a JAK inhibitory nám pomáhají individuální léčbu zaměřenou na pacienta.
MUDr. Jana Hořínková
Revmatologický ústav Praha
