Ovariální karcinom tvoří pouze 5 % všech karcinomů u žen. Ročně je na celém světě diagnostikován u přibližně 295 000 žen. V Česku je nárůst nových případů přibližně 1 000 za rok. Ovariální karcinomy zaujímají dlouhodobě první místo v úmrtnosti na gynekologické nádory. Kvůli příznakům se rakovina vaječníků často nazývá „syndrom malé sukně“. Pro nenápadnost nemoci je většina pacientek diagnostikována v pozdním stadiu, které výrazně zhoršuje prognózu nemoci. Doba do progrese se pohybuje mezi 16–22 měsíci, medián celkového přežití je 2–4 roky a pětileté přežití nedosahuje 30 %. Jde sice o nádor chemosenzitivní, ale ne chemokurabilní a základem léčby zůstává léčba chirurgická.
Vývoj počtu nově diagnostikovaných případů karcinomu vaječníku v České republice ukazuje graf 1.
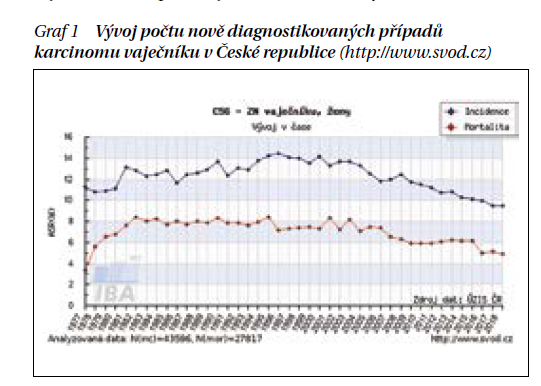
Příčiny vzniku rakoviny vaječníků nejsou přesně známy. Významná role je však přisuzována vlivu estrogenů, dále může hrát roli například obezita. Existují i dědičné formy rakoviny vaječníků, které postihují hlavně mladší ženy do 40 let věku.
Mezi příznaky patří nejasná bolest břicha, trávicí potíže – plynatost, nadýmání, anorexie, nevolnost, zvracení, hubnutí, zejména pokud se současně zvětší obvod břicha; celková slabost, krvácení z pochvy mimo pravidelnou menstruaci či v menopauze. Dále zvětšení obvodu břicha, pokud se zhoubný nádor rozšířil do břišní dutiny a metastazoval do pobřišnice a tvoří se ascites, pocit tlaku na močový měchýř a/nebo střeva, nádor tlačící na močový měchýř nebo střeva může vést k častějšímu nucení na močení než obvykle, případně k zácpě, dušnost.
Typy nádorů: primární nádory vaječníků se dělí do dvou velkých skupin, na nádory epitelové (karcinomy) a nádory vycházející z jiných struktur vaječníků, tzv. neepitelové (např. germinální tumory, nádory z buněk granulózy). Neepitelové nádory postihují obvykle ženy mladšího věku a mají dobrou prognózu, tvoří maximálně 10 % všech nádorů vaječníků. Toto sdělení se věnuje především karcinomu ovarií.
Diagnostické přístupy
Diagnostika zahrnuje anamnézu, gynekologické vyšetření, ultrazvuk, CT či magnetickou rezonanci, dále histologické vyšetření a genetické vyšetření, především ke zjištění somatické či zárodečné mutace genu BRCA. Vyšetřování hladin nádorových markerů (zde hlavně Ca125) má význam spíše při monitoraci efektu léčby.
Léčebné postupy
Léčba nádorů vaječníků a vejcovodů je složitá a kombinovaná, zahrnuje chirurgickou operaci, chemoterapii, cílenou léčbu, hormonální léčbu, ozáření či různé kombinace těchto metod. Prognosticky nejdůležitější je stadium nemoci (graf 2).
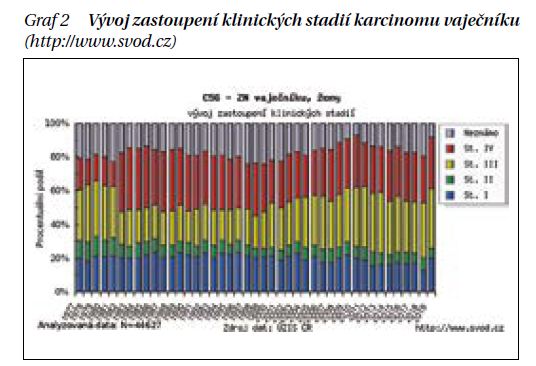
Chirurgie
Základním diagnostickým i léčebných krokem u nádorů vaječníků a vejcovodů je operace provedená zkušeným onkogynekologickým týmem. Podle rozsahu onemocnění pak stanoví optimální postup operace. Je-li onemocnění menšího rozsahu (stadium I, II) a je-li to technicky možné, provede radikální chirurgický výkon, který spočívá v odstranění vaječníků, vejcovodů, dělohy, omenta a slepého střeva, a odeberou se lymfatické uzliny z oblasti pánve a kolem velkých cév.
Někdy ovšem tato radikální operace není možná. Například když nádor postihuje orgány, které by mohl chirurg poranit. Zde chirurg opět odebere vzorek tkáně na histologické vyšetření a snaží se odstranit co nejvíce nádorových hmot (tzv. debulking), byť některé je nucen ponechat v břiše nemocné.
U mladých nemocných, které si přejí mít ještě děti, je možné u velmi časných stadií provést záchovný výkon, který další těhotenství umožní.
Operaci lze provést na začátku léčby pacientky, ale i v odstupu po podání chemoterapie, kdy došlo k výrazné regresi nádoru, tzv. IDS (interval debulking surgery).
Onkologická léčba
Podle stadia nemoci je indikována onkologická léčba. Pouze u stadia IA low grade není po radikální operaci indikována chemoterapie.
Základem chemoterapie jsou tzv. platinové režimy. Lze podat jak monoterapii, tak kombinaci více léčiv. Podle načasování lze chemoterapii rozdělit na neoadjuvantní, kdy se vstupně podají 3–4 cykly chemoterapie a při regresi tumoru následuje operace, po které je znovu podána chemoterapie. Při adjuvantní chemoterapii je po odstranění nádoru podáno standardně 4–6 (až 8) cyklů chemoterapie, nejčastěji kombinace paklitaxel + karboplatina. U pokročilých či metastatických stadií se pak podává paliativní chemoterapie. K dispozici je několik terapeutických linií. Záleží na tom, zda jde ještě o onemocnění platina senzitivní či rezistentní. Další užívaná cytostatika jsou lipozomální doxorubicin, topotekan, docetaxel, gemcitabin, etoposid.
Intraperitoneální chemoterapie se používá pouze na specializovaných pracovištích, kdy je roztok cytostatika zaveden přes katétr do dutiny břišní. Má určitá omezení. Hypertermická intraperitoneální chemoterapie (HIPEC) není standardem léčby ovariálního karcinomu a není indikována v první linii ani pro recidivující onemocnění. Neprodloužila parametry přežití (PFS, OS) a je spojena s toxicitou.
Cílená léčba
Bevacizumab patří mezi anti VEGF, tedy jde o monoklonální protilátku proti endoteliálnímu růstovému faktoru. Důsledkem jeho působení dochází k omezení cévního zásobení nádorových buněk a následně k jejich zániku.
Bevacizumab je hrazen v 1. linii léčby dospělých pacientů s pokročilým karcinomem vaječníků, vejcovodů nebo primárním nádorem pobřišnice (stadia IV podle FIGO nebo stadia III u neoperovaných pacientů nebo stadia III s ˃ 1,0 cm reziduem po operaci) v dávce 7,5 mg/kg každé 3 týdny v kombinaci s karboplatinou a paklitaxelem až po 6 léčebných cyklech, následně se pokračuje v samostatné léčbě bevacizumabem. Léčba bevacizumabem se ukončuje při zjištění progrese či při netoleranci léčby, nejdéle po 12 měsících (18 cyklech) léčby podle toho, co nastane dříve. Dále je bevacizumab hrazen v kombinaci s paklitaxelem k léčbě dospělých pacientek se stavem výkonnosti 0–1 podle ECOG s rekurencí epitelového nádoru vaječníků, vejcovodů nebo primárního nádoru pobřišnice rezistentního k platině (tj. pokud došlo k progresi do 6 měsíců po ukončení terapie na bázi platiny), které nebyly léčeny více než dvěma předchozími režimy chemoterapie a nebyly dosud léčeny bevacizumabem nebo jiným inhibitorem růstového faktoru cévního endotelu (VEGF) nebo receptoru VEGF. Léčba je hrazena do progrese onemocnění.
Další možností je terapie inhibitory PARP, tj. léky, které blokují poly (ADPribóza) polymerázu (PARP), což je enzym, který pomáhá opravovat poškozenou DNA.
Každá pacientka s epiteliálním ovariálním karcinomem bez ohledu na věk, histotyp a rodinnou anamnézu je indikována k vyšetření germinálních (gBRCA), optimálně i somatických (sBRCA) mutací genů BRCA1 a BRCA2.
Každá pacientka s pokročilým high-grade serózním nebo high-grade endometroidním karcinomem ovaria, která nemá progresi onemocnění po dokončení chemoterapie po primární nebo intervalové debulkingové operaci, by měla být léčena PARP inhibitory v udržovací léčbě.
Oba aktuálně dostupné PARP inhibitory (olaparib a niraparib) prokázaly účinnost u pacientek s germinální i somatickou mutací genů BRCA1/2, niraparib má k dispozici data účinnosti i v neselektované populaci pacientek. Léčbu olaparibem je nutné zahájit do 8 týdnů od ukončení chemoterapie a trvá do netolerovatelné toxicity, progrese onemocnění nebo maximálně po dobu 2 let. Léčbu niraparibem je nutné zahájit do 12 týdnů od ukončení chemoterapie a trvá do netolerovatelné toxicity, progrese onemocnění nebo maximálně po dobu 3 let. Oba přípravky mají mírně odlišný profil toxicity, dosud nejsou k dispozici komparativní studie obou preparátů. Studie prokázaly výrazné zlepšení PFS i OS při nasazení PARP inhibitoru do první linie léčby, a to hlavně u BRCA mutovaných nemocných.
Lynparza (olaparib) v kombinaci s bevacizumabem je indikován pro udržovací léčbu pacientek s pokročilým high grade epiteliálním karcinomem vaječníků, vejcovodu nebo primárním peritoneálním karcinomem (FIGO III a IV), které dosáhly odpověď (úplnou, nebo částečnou) po dokončení první linie chemoterapie na bázi platiny a které mají potvrzený deficit homologní rekombinace (HRD) definovaný mutací BRCA 1, BRCA 2 a/nebo genomovou nestabilitou.
Pro serózní karcinom vaječníků je typická častá recidiva nemoci, nárůst rezistence k léčbě a postupné zkracování času do další progrese nemoci.
Mezi další terapeutické možnosti patří paliativní ozáření například bolestivých kostních metastáz či metastáz v CNS apod., dále podávání bisfosfonátů u kostních metastáz, paliativní hormonální terapie, například u ER pozitivních nádorů, nutriční terapie, analgoterapie a psychologická podpora pacientek při pokročilých stadiích nemoci.
Kazuistika
Pacientka, ročník 1967, byla poprvé vyšetřena na našem oddělení v dubnu 2019. Byla odeslána z gynekologie pro karcinom ovarií (obrázek 1). Po vyšetření MR a UZ byla následně dne 25. 3. 2019 provedena hysterectomia abdominalis cum adnexectomia bilateralis, cytologie, částečná resekce omenta, ponecháno reziduum. Podle MR břicha předoperačně bez výraznějšího postižení intraperitoneálně.
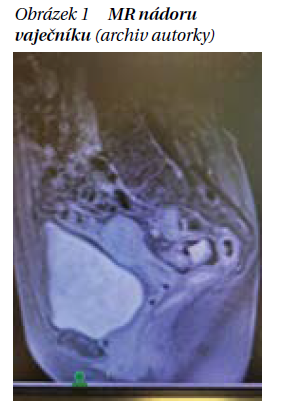
Podle operačního protokolu: V celé dutině břišní metastatický rozsev, játra na povrchu s metastázami – ponecháno reziduum. CA 125: 218,9 předoperačně. Pooperační markery: CA 125: 128,3.
Staging: Ca ovarii pT3acN0MX/1, hist: high grade serózní karcinom.
Pacientka astenická, léčila se jen s Crohnovou nemocí, měla tedy potíže se stolicí po operaci střev.
MDT byla indikována k pooperační chemoterapii vzhledem k operačnímu nálezu 6–8 cykly paklitaxel + karboplatina.
Chemoterapii snášela s neurotoxicitou a hematotoxicitou. Absolvovala celkem 8 cyklů od dubna do října 2019. Zároveň absolvovala i genetické vyšetření a byla jí prokázána mutace genu BRCA1.
Kontrolní restaging neprokázal progresi onemocnění a pacientka byla indikována k léčbě olaparibem (Lynparza tbl.). Léčba byla nasazena v listopadu 2019. Snášela ji s únavou, měla i chronické potíže se stolicí, jinak dobře. Na neuropatie po předchozí léčbě paklitaxelem jí byl nasazen gabapentin tablety. Postupně se objevila i anémie, ale bez nutnosti podání krevních převodů. Na léčbě byla do konce října 2021, tedy 2 roky. Poté jí byla pro trvající kompletní remisi léčba ukončena. Po celou dobu léčby pacientka užívala plnou dávku léku 300 mg 2× denně.
Následně sledována. V dubnu 2022 jí byla pro genetickou zátěž provedena i profylaktická oboustranná mastektomie. Poslední CT vyšetření měla v listopadu 2023 s trvající kompletní remisí nemoci. Nyní je 4 roky a 9 měsíců od operace a je zdravá.
Závěr
Důležité pro rozhodování o léčbě je kromě stadia nemoci a možnosti operability také celkový stav pacientky, věk, komorbidity a přání pacientky. Nezastupitelný je pak multidisciplinární tým pro gynekologické tumory. Velkým přínosem v léčbě jsou inhibitory PARP, které oddalují progresi nemoci a prodlužují i celkové přežití pacientek.
MUDr. Jana Pukyová
KOC, Masarykova nemocnice v Ústí nad Labem, o. z.
