Léčba průduškového astmatu v posledních desetiletích zaznamenala několik velmi významných milníků. Zavedení topické léčby inhalačními kortikoidy a následně kombinované terapie inhalační kortikoterapie a dlouhodobě účinkující bronchodilatační terapie v kombinovaných přípravcích zásadně změnilo kvalitu života naprosté většiny pacientů. I když jsou úspěchy této léčby nesporné, zůstává část pacientů, u kterých je topická terapie nedostatečná. Jedná se o skupinu pacientů trpících nejzávažnější formou astmatu, těžkým asthma bronchiale.
Těžké astma je formou astmatu, která k dosažení kontroly vyžaduje středně vysoké nebo vysoké dávky inhalačních kortikosteroidů v kombinaci s bronchodilatační terapií s prodlouženým uvolňováním a často i další terapií (antileukotrieny, teofyliny). V některých případech ale ani tato terapie nestačí k dosažení kontroly nemoci. Pak se jedná o dvě klinické situace:
Obtížně léčitelné astma (OLA): u těchto nemocných není důvodem nedostatečné kontroly tíže astmatu samotného, ale nepoznané anebo nedostatečně léčené komorbidity. Jedná se zejména o kardiovaskulární nemoci, obezitu, GERD a další. Komplikujícími faktory mohou být přetrvávající expozice alergenem, kouření, nedostatečná adherence k léčbě, špatná inhalační technika a podobně. V těchto případech je nejdůležitější řešení komplikujících faktorů, dostatečná léčba komorbidit, zlepšení adherence k léčbě, odstranění alergenů a léčba závislosti na tabáku.
Těžké refrakterní astma (TRA): u těchto nemocných je důvodem nedostatečné kontroly tíže nemoci samotné. Ani při adekvátní adherenci pacienta, optimální léčbě komorbidit, eliminaci komplikujících faktorů a vysoké dávce kombinované topické léčby nedochází k dosažení dostatečné kontroly nemoci. V této situaci je často nutné sáhnout po léčbě systémovými kortikoidy se všemi jejich nežádoucími účinky. Moderní management léčby upřednostňuje před léčbou systémovými kortikoidy biologickou léčbu. Tato léčba vychází z lepšího poznání patofyziologie astmatu. Je víc cílená proti strukturám podílejícím se na patogenezi onemocnění. Cílem je dosáhnout lepší kontroly onemocnění a současně snižovat dávky anebo vynechat terapii systémovými kortikoidy. Dosahuje se tak eliminace nežádoucích účinků kortikoidů. Pro optimální volbu biologické terapie je důležité stanovit fenotyp astmatu. Stupňovitou terapii podle závažnosti astmatu podle doporučení GINA lze nalézt na http://www.ginasthma.org.
Fenotypy astmatu
V patofyziologii astmatu se uplatňují 3 základní fenotypy:
- eozinofilní alergické astma;
- eozinofilní nealergické astma;
- non eozinofilní nealergické astma.
Fenotyp I a II bývá označován rovněž jako Th2 high zánět. Rozhodující roli zde hrají cytokiny produkované Th2 lymfocyty. Jedná se o interleukiny IL-4, IL- 5 a IL-13. Výsledky výzkumů ukazují, že přibližně 75 % pacientů s těžkým astmatem patří do těchto dvou skupin.
Třetí skupina – non eozinofilní nealergické astma – bývá označována jako Th2 low zánět. Zde hrají významnou roli neutrofily, IL-6 a thymický stromální lymfopoetin TSLP.
Jednotlivá biologika, monoklonální protilátky, cílí právě proti jednotlivým mediátorům zánětu. Znalost převládajícího fenotypu u konkrétního nemocného umožňuje optimální volbu nejvhodnějšího biologika.
Biologická léčba astmatu
Biologická léčba těžkého astmatu přinesla skutečnou revoluci v léčbě nejtěžších forem nemoci. První protilátka omalizumab byla do klinické praxe v ČR uvedena v roce 2008, následoval mepolizumab a reslizumab v roce 2018, v roce 2019 benralizumab a v roce 2022 dupilumab. Posledním biologikem je od roku 2023 v ČR dostupný tezepelumab.
Biologická léčba zlepšuje kontrolu nemoci, snižuje počet těžkých exacerbací a snižuje potřebu podávání systémové kortikoterapie. U pacientů, kteří jsou již systémovými kortikoidy léčeni, často vede ke snižování dávky kortikoidů. U některých nemocných můžeme dosáhnout úplného vysazení systémové kortikoterapie. Včasné nasazení biologické léčby může předejít nutnosti trvalé systémové kortikoterapie.
Všechny přípravky biologické léčby astmatu jsou dostupné jen v injekční formě. Velkou výhodou většiny z nich je možnost aplikace pacientem v domácím prostředí formou předplněných injekcí „home use“. To zlepšuje compliance pacientů a snižuje počet nutných návštěv v ambulanci.
Dostupná biologika
Omalizumab – anti IgE protilátka je humanizovaná monoklonální protilátka, která se selektivně váže na lidský imunoglobulin E (IgE). To způsobuje pokles cirkulujících IgE a potlačení exprese vysokoafinitních receptorů pro IgE na bazofilech, žírných a dendritických buňkách. Výsledkem je následně zlepšení projevů nemoci u pacientů s převažujícím eozinofilním alergickým fenotypem. Podmínkou úhrady je prokázané alergické astma, alergie na celoroční vzdušný alergen, 2 těžké exacerbace za posledních 12 měsíců, hladina IgE 30–1 500 IU/ml (6–11 let) anebo 30–700 IU/ml (nad 12 let věku). Na našem trhu je dostupný přípravek Xolair. Právě s touto léčbou jsou největší zkušenosti.
Mepolizumab (preparát Nucala), reslizumab (preparát Cinqaero) – anti-IL5 protilátky jsouhumanizované monoklonální protilátky vyráběné na ovariálních buňkách čínských křečků rekombinantní DNA technologií. Inhibují biologickou aktivitu interleukinu IL-5 blokováním vazby IL-5 na alfa řetězec komplexu IL-5 receptoru umístěného na povrchu eozinofilní buňky. Inhibují signalizační funkci IL-5 a snižují produkci a přežití eozinofilů. Léčba je indikována u pacientů, u kterých je prokázáno těžké eozinofilní astma, absolutní počet eozinofilů v periferní krvi je nejméně 300/mikrolitr u mepolizumabu a 400/mikrolitr u reslizumabu. Dále mají dokumentované nejméně 4 těžké exacerbace astmatu v průběhu 12 měsíců před zahájením léčby, anebo užívají perorální kortikosteroidy v dávce ekvivalentní nejméně 5 mg prednisonu denně po dobu alespoň 6 měsíců před zahájením léčby.
Benralizumab (preparát Fasenra) – anti-IL-5Ralfa protilátka je humanizovaná monoklonální protilátka (IgG1, kapa). Váže se na alfa podjednotku receptoru pro lidský interleukin 5 (IL-5Ralfa). Receptor IL-5 je specificky exprimován na povrchu eozinofilů a bazofilů. To vede k apoptóze eozinofilů a bazofilů a ke snížení jejich absolutního počtu v periferní krvi. Výsledkem je snížení intenzity eozinofilního zánětu. Pacienti jsou k léčbě indikováni, pokud je u nich prokázáno těžké eozinofilní astma, absolutní počet eozinofilů je nejméně 300/mikrolitr periferní krve a mají dokumentované nejméně 4 těžké exacerbace astmatu v průběhu 12 měsíců před zahájením léčby, anebo užívají perorální kortikosteroidy v dávce ekvivalentní nejméně 5 mg prednisonu denně po dobu alespoň 6 měsíců před zahájením léčby.
Dupilumab (preparát Dupixent) – anti-IL-4/IL-13 protilátka je rekombinantní lidská monoklonální protilátka třídy IgG4, která inhibuje signální dráhu interleukinu IL-4 a interleukinu IL-3. Blokování dráhy IL-4/IL-13 dupilumabem vede u pacientů k poklesu řady mediátorů zánětu typu Th2 high. Léčba je indikována u pacientů s prokázaným těžkým eozinofilním astmatem, absolutní počet eozinofilů je nejméně 300/mikrolitr periferní krve a mají dokumentované nejméně 4 těžké exacerbace astmatu v průběhu 12 měsíců před zahájením léčby anebo užívají perorální kortikosteroidy v dávce ekvivalentní nejméně 5 mg prednisonu denně po dobu alespoň 6 měsíců před zahájením léčby.
Tezepelumab (přípravek Tezespire) – anti-TSLP protilátka je humanizovaná monoklonální protilátka. Váže se na tymický stromální lymfopoetin (TSLP), čímž blokuje jeho vazbu na receptor pro TSLP. FDA schválila tezepelumab pro léčbu těžkého astmatu napříč fenotypy bez ohledu na biomarkery. V ČR je nyní dostupná v programu časného přístupu po schválení revizním lékařem plátce.
Které biologikum u kterého pacienta zvolit?
Velmi důležité pro optimální volbu nejlepšího biologika je vycházet z fenotypu pacienta.
U některých pacientů se fenotypy mohou překrývat. Je proto nutné zvážit převládající typ fenotypu u každého jedince individuálně. Dostupnost vícerých preparátů s různým mechanizmem účinku a cílovou strukturou nám dává možnost switch terapie mezi jednotlivými preparáty (musí ale vždy splňovat podmínky úhrady). To umožňuje hledat nejlepší možnou léčbu i u pacientů, kteří na dosavadní terapii nezareagovali dostatečně. K lepší orientaci pomáhá i stanovení biomarkerů: hladina IgE, absolutní počet Eo, FeNO. Jejich znalost zlepšuje přesnost určení fenotypu astmatu.
Vhodné je zvažovat i způsob aplikace (s. c., i. v., home use), který je pro konkrétního pacienta nejvhodnější.
Roli mohou sehrát i speciální situace, např. vysoká hmotnost pacienta a vysoká hladina IgE u konkrétního pacienta mohou vést k nutnosti aplikovat vysoké dávky omalizumabu. V těchto případech, pokud je to možné, je vhodné volit jiné biologikum.
Organizace biologické léčby v ČR
Biologická léčba těžkého astmatu je v ČR soustředěna do Center pro těžké astma (jejich seznam je dostupný na https://www.tezke-astma.cz). Jedná se o léčbu centrovou, proto v jiných zařízeních není možná.
Kdy odeslat pacienta do centra?
Doporučené postupy pro léčbu astmatu ČPFS a ČSAKI uvádí: V případě, že se nedaří uvést astma pod kontrolu léčbou na úrovni 4. stupně, před eventuálním nasazením dlouhodobé systémové kortikoterapie, doporučujeme nemocného odeslat do centra pro těžké astma. Léčba pacientů s obtížně léčitelným astmatem vyžaduje zkušenosti, individuální přístup, dostupnost náročných vyšetřovacích metod a dobrou mezioborovou spolupráci. Tyto nemocné je vhodné odeslat do specializovaného vyššího centra, které je schopné realizovat došetření komplikujících faktorů astmatu a posoudit další možnosti jeho léčby. Algoritmus rozhodování o odeslání pacienta do centra ukazuje schéma 1. Podobně je doporučeno postupovat při zvažování zahájení biologické terapie i v dokumentu GINA (dostupné na http://www.ginasthma.org).
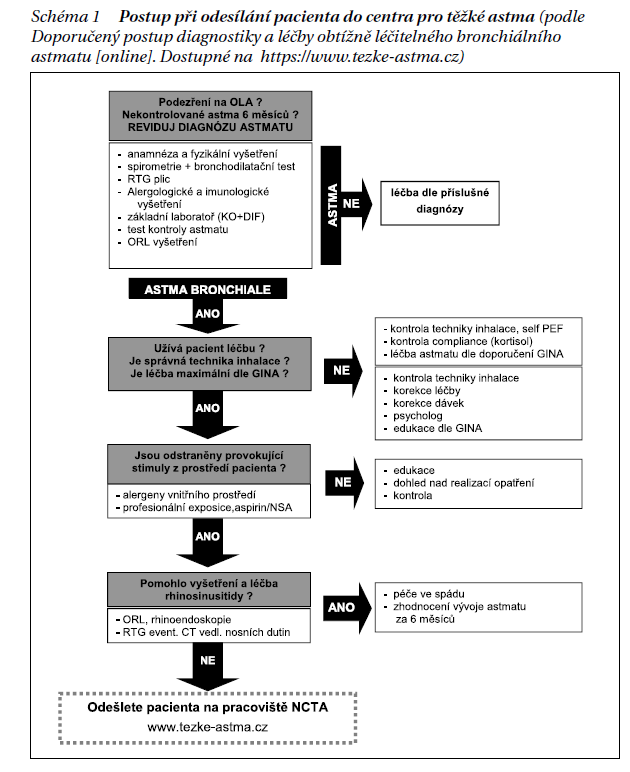
Pro terapeutickou rozvahu je nutné mít k dispozici dokumentované hladiny krevních eozinofilů alespoň 12 měsíců před eventuálním zahájením biologické léčby. Dále stanovení hladiny IgE, vyšetření specifických IgE nebo prick testů. Nutná je dokumentace počtu exacerbací ve zdravotnickém zařízení.
Závěr
V oblasti biologické terapie těžkého astmatu dochází k výraznému pokroku. Prakticky rok od roku přicházejí nová a nová biologika cílící na různé mechanizmy v patofyziologii astmatu. Rozšiřuje se tak možnost optimálního nastavení nejlepší léčby pro konkrétního pacienta. Stoupá i počet pacientů, kteří jsou úspěšně léčeni bez ohledu na tíži svého onemocnění. Naopak postupně klesá počet pacientů, kterým zatím adekvátní léčbu nemůžeme nabídnout.
MUDr. Gustáv Ondrejka, Ph.D.
Plicní oddělení KNTB Zlín
