Na výročním zasedání ASCO 2023 GU letos v únoru v rámci sekce věnované pokročilému karcinomu prostaty, konkrétně novým cílům a výzvám v této terapeutické oblasti a také novým lékům, vystoupila Dr. Maha Hussain s prezentací o účinnosti a bezpečnosti darolutamidu v kombinaci s androgenní deprivační terapií (ADT) a docetaxelem podle objemu onemocnění a podle rizika onemocnění zkoumaných ve studii ARASENS fáze 3. Výsledky uvedené studie prokázaly, že darolutamid plus ADT v kombinaci s docetaxelem významně snižuje riziko úmrtí o 32,5 % ve srovnání s ADT s docetaxelem, a to u pacientů s metastatickým hormonálně senzitivním karcinomem prostaty (mHSPC)3.
Právě na základě údajů z uvedené klinické studie schválila Evropská komise přípravek NubeqaTM (darolutamid) pro léčbu těchto pacientů.
Rakovina prostaty je celosvětově druhým nejčastěji diagnostikovaným zhoubným onemocněním u mužů a nejčastějším onkologickým onemocnění u mužů v České republice. Incidence karcinomu prostaty stoupá s věkem, před 40. rokem se téměř nevyskytuje, naopak mezi 65. a 75. rokem života je výskyt nejvyšší[i]. V roce 2020 bylo podle odhadů diagnostikováno 1,4 milionu mužů s karcinomem prostaty a přibližně 375 tisíc jich na toto onemocnění celosvětově zemřelo[ii].
Metastatický hormonálně senzitivní karcinom prostaty
V době diagnózy má většina mužů lokalizovanou rakovinu prostaty, která může být léčena kurativním chirurgickým zákrokem nebo radioterapií. Při relapsu, kdy onemocnění metastazuje nebo se rozšíří, nebo pokud je onemocnění nově diagnostikováno, je choroba hormonálně senzitivní a základem léčby je ADT.
Současné možnosti léčby mužů s mHSPC zahrnují hormonální léčbu, například ADT, inhibitory dráhy androgenních receptorů plus ADT nebo kombinaci ADT a docetaxelu. Navzdory této léčbě u velké části mužů s mHSPC nakonec dojde k progresi do metastatického kastračně rezistentního karcinomu prostaty (mCRPC), což je stav s vysokou morbiditou a omezeným přežitím.
Studie ARASENS fáze 3
Studie ARASENS je jediná randomizovaná, multicentrická, dvojitě zaslepená studie fáze 3, která byla prospektivně navržena tak, aby porovnávala použití perorálního inhibitoru androgenních receptorů (ARi) druhé generace darolutamidu plus ADT v kombinaci s docetaxelem a léčbou ADT plus docetaxel u mHSPC.
Pacienti s mHSPC byli randomizováni v poměru 1 : 1 k užívání darolutamidu 600 mg dvakrát denně nebo placeba s ADT + docetaxelem. Uspořádání studie ARASENS je uvedeno na obrázku 1.

Onemocnění s velkým objemem bylo definováno jako viscerální metastázy a/nebo 4 a více kostní metastázy, z nichž 1 a více přesahovala páteř/pánev (podle kritérií CHAARTED). Vysoce rizikové onemocnění bylo definováno na základě přítomnosti 2 a více rizikových faktorů:
- Gleasonovo skóre ≥ 8;
- ≥ 3 kostní léze;
- přítomnost měřitelných viscerálních metastáz (kritéria LATITUDE).
Celkové přežití těchto podskupin bylo hodnoceno pomocí nestratifikovaného Coxova regresního modelu.
Výsledky
Primárním cílovým ukazatelem studie ARASENS bylo celkové přežití (OS). Sekundární cílové ukazatele studie zahrnovaly dobu do vzniku CRPC, dobu do progrese bolesti, dobu do první symptomatické skeletální příhody (SSE), dobu do zahájení následné protinádorové léčby. Sledovány byly rovněž nežádoucí účinky jako měřítko bezpečnosti a snášenlivosti léčby.
Darolutamid + ADT + docetaxel prodloužily celkové přežití bez ohledu na onemocnění s vysokým nebo nízkým objemem – konkrétně pro mHSPC s velkým objemem (HR 0,69, 95% CI 0,57–0,82) a mHSPC s malým objemem (HR 0,68, 95% CI 0,41–1,13). Křivky celkového přežití pro mHSPC s vysokým rizikem (HR 0,71, 95% CI 0,58–0,86) a mHSPC s nízkým rizikem (HR 0,62, 95% CI 0,42–0,90) jsou uvedeny v grafu 1.
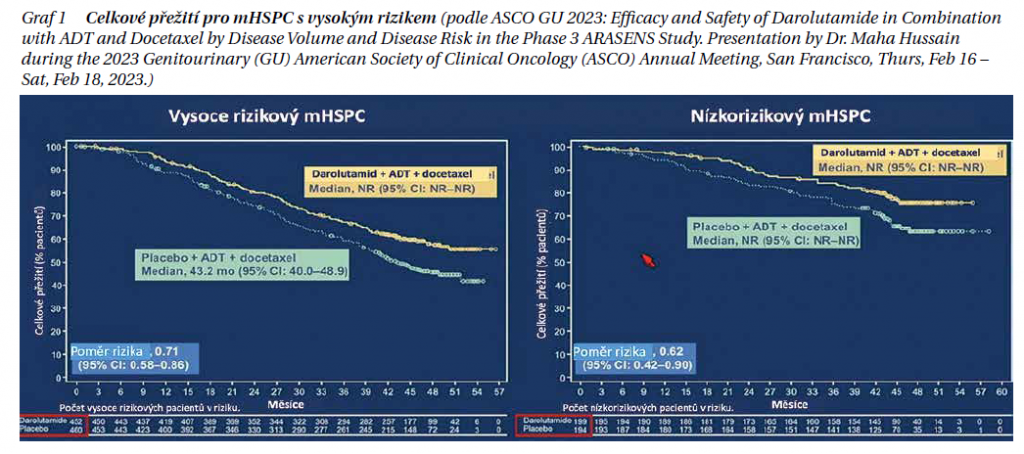
Pokud jde o dobu do vzniku CRPC, z tripletové terapie profitovali pacienti s vysokým i nízkým objemem a s vysokým i nízkým rizikem onemocnění.
Oproti placebu darolutamid zlepšil klinicky relevantní sekundární koncové ukazatele studie v podskupinách s vysokým/nízkým objemem a rizikem, přičemž poměry rizik se obecně pohybovaly v rozmezí hodnot přítomných v celkové populaci.
Výskyt nežádoucích účinků vyvolaných léčbou byl konzistentní s celkovou populací ARASENS v podskupinách podle velkého/malého objemu a vysokého/malého rizika.
Závěry
Přednášející zakončila prezentaci výsledků studie ARASENS o účinnosti a bezpečnosti darolutamidu v kombinaci s ADT a docetaxelem podle objemu a podle rizika onemocnění následujícími závěry:
- U pacientů s mHSPC byl přínos časné intenzifikace léčby darolutamidem + ADT + docetaxelem na celkové přežití a klíčové sekundární cíle studie účinnosti relevantní pro pacienta ve srovnání s placebem + ADT + docetaxelem konzistentní u pacientů s mHSPC s vysokým i nízkým objemem onemocnění a s vysokým i nízkým rizikem.
- Příznivý bezpečnostní profil darolutamidu byl znovu potvrzen u populací s vysokým/nízkým objemem a vysokým/nízkým rizikem.
- Darolutamid + ADT + docetaxel tak stanovuje nový standard péče o pacienty s mHSPC.
Ve studii ARASENS darolutamid plus ADT a docetaxel oproti placebu + ADT + docetaxelu významně snížil riziko úmrtí o 32,5 % (HR 0,68; 95 % CI 0,57–0,80) u pacientů s mHSPC, přičemž celková incidence nežádoucích účinků způsobených léčbou byla mezi skupinami podobná[iii]. Účinek darolutamidu na celkové přežití byl konzistentní napříč předem specifikovanými podskupinami, včetně de novo a rekurentního onemocnění. U pacientů s mHSPC poskytují výsledky založené na objemu onemocnění a riziku další důležité informace pro léčbu tohoto onemocnění.
Prezentováno Maha H. A. Hussain, MD, FACP, FASCO, Northwestern University, Feinberg School of Medicine, Chicago, IL, na výročním kongresu 2023 GU ASCO, San Francisco, USA
Mgr. Milan Krenželok, Dr.
[i] www.mou.cz
[ii] Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. Cancer J Clin. 2021; 71: 209–249.
[iii] Smith MR, Hussain M, Saad F, et al. Darolutamide and Survival in Metastatic, Hormone-Sensitive Prostate Cancer. N Engl J Med. 2022; 386(12): 1132–1142.
