Luhačovické Diabetologické dny, již tradičně pořádané v průběhu dubna, se konaly vlivem epidemiologické situace opět v online prostoru. V rámci jejich 57. ročníku mezi jednotlivými přednáškami, přenášenými ve dnech 14. – 16. 4. 2021, proběhlo i sympozium sponzorované firmou Viatris, zaměřené na posouzení nového glarginového biosimilars Semglee.
Úvodu se zhostil profesor MUDr. Milan Kvapil, CSc., MBA, přednosta Geriatrické interní kliniky 2. LF UK a FN Motol. V krátkosti nastínil základní fyziologické principy i historická fakta. Je již všeobecně známo, že inzulin zastává v organismu mnoho důležitých funkcí. V mládí funguje jako anabolikum v rámci růstu organizmu, celoživotně se potom účastní metabolizmu glukózy, tuků a mastných kyselin. Zlomovým objevem bylo, že jeho sekrece se ve zdravém organizmu řídí aktuální potřebou.
Od objevu inzulinu do současnosti
Za objevem inzulinu stojí sir Frederick Grant Banting, kanadský lékař, který spolu s Charlesem Bestem izoloval tento hormon ze slinivky břišní a popsal jeho účinky. Od chvíle, kdy jsme schopni ho v těle nahradit, lidé neumírají zpravidla na diabetes jako takový, ale na jeho nejčastější komplikace. Řada z nich je ovšem způsobena vlastní léčbou inzulinem. Jak v historických dobách, tak i dnes diabetiky nejvíce ohrožuje hypoglykémie či hyperglykémie při nesprávném dávkování, dále jsou to septické stavy nebo akcentovaná ateroskleróza a její následky.
K pochopení fyziologické sekrece a jejího rytmu odvislého od příjmu potravy došlo v průběhu šedesátých let. Z této doby také pochází nová schémata aplikace, první senzory, snahy o edukaci pacienta s výsledným zlepšením kompenzace, což vše v kombinaci vedlo k menšímu výskytu hyperglykemických a hypoglykemických epizod. K dispozici ovšem tehdy nebyly inzuliny, jaké máme dnes, ale zvířecí analoga, povětšinou hovězí a vepřový inzulin. Vepřový, vzhledem ke své struktuře, která se jen o jednu aminokyselinu liší od humánního, byl o něco vhodnější. Humánní inzuliny syntetizované pomocí bakterií či kvasinek přišly až o něco později. Jak vývoj pokračoval, kromě animálních a humánních se postupem času dostalo i na lidská analoga. Prvními byly detemir a glargin, které se liší mechanismem účinku i jeho délkou a potřebným množstvím k dosažení stejného efektu. Ze statistik vidíme, že terapeuticky se postupně v posledních deseti letech přikláníme stále více k terapii lidskými analogy pro jejich zjevné výhody, mezi které patří například velmi vzácně vzniklé alergické reakce. Do nové éry patří i tzv. biosimilars, verze již existujících biologických léků u nichž vypršela patentová ochrana.
Biosimilární glargin
„Semglee je biosimilární inzulin – glargin podobný originálnímu léku, ale není identický, tj. nejedná se o generikum.“ Ujasnila na začátku druhé části doc. MUDr. Alena Šmahelová, Ph.D. z III. Interní gerontometabolické kliniky Fakultní nemocnice v Hradci Králové.
Výroba biosimilars je obecně složitá, mnohastupňová a dochází během ní k modifikaci základního molekuly, nejčastěji bílkoviny. Získaná data ukazují, že Semglee má s glarginem shodnou farmakodynamiku a farmakokinetiku a lze jej považovat za ekvivalentní variantu v terapii cukrovky.
První ze studií, která se porovnáním biosimilars s původním lékem (Lantus) zabývala, byla crossover studie u diabetu mellitu 1. typu (DM1). V základu měla tři ramena; Lantus vyrobený v USA, Lantus vyrobený v Evropě a Semglee. Základní metodikou byl euglykemický clamp s trváním 30 hodin a cílovou glykémií okolo 4,5 mmol/l. Inzulin byl v dávce 0,4 U/kg. Pacienti museli splňovat vstupní kritéria:
- věk 18-55,
- BMI 18,5-30kg/m2,
- HbA1c < 9 %,
- denní potřeba inzulinu < 1,4 U/kg/den,
- C-peptid nalačno s 0,3 pmol/mL.
Z grafu 1 je zjevné, že farmakokinetický i farmakodynamický profil všech použitých preparátů si vzájemně odpovídá na základě porovnání hladin metabolitu M1.
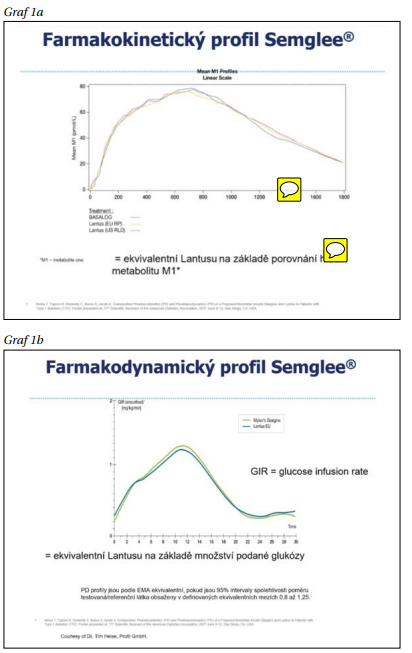
Klinicky je velice zajímavé srovnání efektivity a bezpečnosti. V případě Semglee se u diabetiků této problematice věnovaly hned dvě studie, a to INSTRIDE 1 (DM1) a INSTRIDE 2 (DM2).
V rámci INSTRIDE 1 byl primárním end-pointem celkový glykovaný hemoglobin. Křivka na grafu 2 ukazuje, že Semglee a Lantus se nijak neliší. Nežádoucí účinky se u obou preparátů vyskytují ve srovnatelném množství. Nejčastějším a pro diabetes, respektive aplikaci inzulinu, byla specifickým nežádoucím účinkem hypoglykémie. Jedním ze sekundárních end-pointů bylo také zjištění ekvivalentní účinnosti stejných dávek, které se potvrdilo.
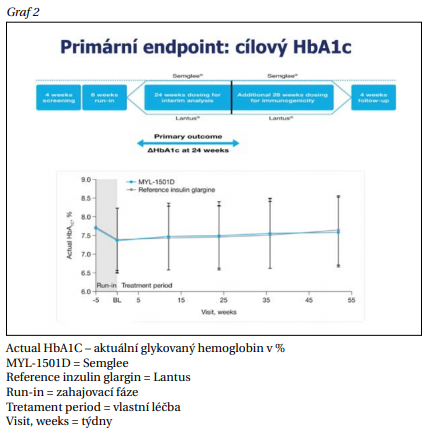
INSTRIDE 2 zaměřená na diabetiky 2. typu měla jako cílový end-point také hladinu glykovaného hemoglobinu. I v této studii se potvrdila shodná účinnost obou léků, srovnatelné zastoupení NÚ a shodné dávkování. Obě studie tedy prokázaly, že Semglee je non-inferiorní proti originálu.
Poslední studií se shodným názvem je INSTRIDE 3, navržená jako multicentrická, otevřená, randomizovaná switch studie porovnávající účinnost a bezpečnost Semglee v kombinaci s jiným glarginem (Lantus) a v poledne ještě dávka krátkého inzulinu (Lispro). Primárním cílem bylo zjištění, zda mohou být pacienti s cukrovkou 1. typu převedeni ze Semglee na glargin během hodnocení ekvivalence po dobu 36 týdnů. I tato studie vyšla pozitivně.
Proč vlastně mít léky, které fungují stejně dobře jako jiné léky?
Na výše uvedenou otázku sepokusilodpověď ve třetí části sympozia MUDr. Tomáš Doležal, Ph.D. Faktem je, že nové léky, které jsou podobné těm již dostupným, budou levnější a zlevní léčbu diabetiků celkově. Nové biosimilární preparáty snižují náklady na terapii, a to i starším alternativám, přibližně o 30 % již v momentě vstupu na trh. To je něco, co naše zdravotnictví v situaci, kdy pod diagnózou některého typu diabetu máme zařazených více jak 1 milion osob, jednoznačně potřebuje. S takovým číslem totiž cukrovka představuje jeden z největších zdravotních problémů v ČR.
Matematické modely dokládají, že náklady na DM se blíží k 20 % nákladů na zdravotnictví. Nákladnost samozřejmě roste s pokračujícím věkem, intenzifikací terapie a horší kompenzací. Data ze studie se 70 000 pacienty z jedné menší pojišťovny ukazují, že počet diabetiků roste. Mnohem rychleji, než počet diabetiků, ovšem rostou náklady jak průměrné, tak celkové. Největší objem celkové částky připadá na řešení komplikací DM – nutnost hospitalizace, intenzivní péče, výjezdy záchranné služby aj. Prostředky vynaložené na diabetika rostou s výskytem přidružených onemocnění a komplikací. To jsou data, která by pojišťovny měla motivovat k tomu, aby nekrátily iniciální náklady na terapii.
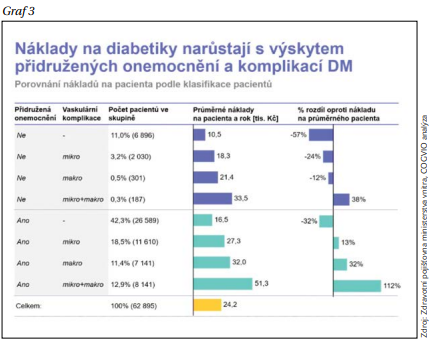
Snižování nákladů na základě dostupnosti generik není novinkou. Za deset let díky vstupu alternativ různých léků na trh přesáhly úspory 33 miliard, největším podílem přispěly statiny a ACE inhibitory. Snahou bylo získat obdobná data z pohledu biosimilars. Ta se dostanou do ČR rychle ve srovnání s původními léky. Potenciál poklesu ceny vstupem nového preparátu na trh je poměrně dobře zvládnutý. U EMA je registrovaných 31 biosimilárních léků, u nás je dostupných celkem 23 z nich. Analýzou dat se došlo k závěru, že biosimilars uspořila přes 6 miliard korun a v následujících letech se dá očekávat nárůst tohoto čísla. Největší úspory jsou v oblasti monoklonálních protilátek anti-TNF. Velký smysl má zachování finanční udržitelnosti trhu a uvolnění prostředků pro nové inovativní léky. Ekonomický faktor klinikům často uniká, ale výše uvedená čísla jednoznačně ukazují, že je na místě se pravidelně informovat a nové preparáty u pacientů využívat.
MUDr. Lucie Hoznauerová
