Tepenný a žilní systém se odlišují svými anatomickými, strukturálními i funkčními vlastnostmi. Oba systémy jsou však provázané a lze najít i některé společné rysy a vzájemné asociace. Učíme se rozlišovat arteriální a žilní trombózu. Nicméně antikoagulancia, používaná k léčbě žilní tromboembolické nemoci, jsou vysoce účinná v prevenci arteriálního embolizmu u pacientů s fibrilací síní. Antiagregancia, indikovaná k léčbě a prevenci arteriální trombózy, jsou do jisté míry účinná i v prevenci žilního tromboembolizmu.
I přes zjevnou rozdílnost existují souvislosti mezi tepennými a žilními chorobami, což potvrzují epidemiologické studie, základní a klinický výzkum i zkušenosti z praxe. Nedávná Gutenberg Health Study dokonce zjistila u jedinců s chronickou žilní insuficiencí nejen vyšší prevalenci kardiovaskulárních chorob, ale i zvýšení mortality ze všech příčin. Cévní onemocnění tedy vyžadují komplexní přístup.
Epidemiologické studie
Souvislosti mezi onemocněními žil a tepen lze demonstrovat např. na výsledcích epidemiologických studií zaměřených na skupiny jedinců s postižením žil.
Nemocní s neprovokovanou žilní tromboembolickou příhodou měli vyšší výskyt aterosklerotických plátů v karotidách, v několika studiích měli během následného follow-up vyšší výskyt kardiovaskulárních příhod.
Nemocní s varixybyli sledováni v rámci Framinghamské studie (3 822 jedinců s varixy) a měli vyšší incidenci kardiovaskulárních chorob,v tchaiwanské retrospektivní studii (212 984 pacientů s varixy a 212 984 kontrol) měli po dobu sledování (medián 7,5 roku) vyšší incidenci nejen žilní tromboembolické nemoci(TEN), ale i ischemické choroby dolních končetin (ICHDK),ve finské prospektivní studii byli jedinci s varixy (4 903 pacientů) sledováni po dobu pěti let a oproti kontrolám byl u nich zjištěn vyšší výskyt ICHDK, ischemické choroby srdeční (ICHS) a cévní mozkové příhody (CMP).
Nemocní s defekty dolních končetin mají až ve 26 % smíšenou etiologii, tj. současně žilní insuficienci a ICHDK.
Etiopatogenetické souvislosti
Otázkou je, zda příčinou těchto souvislostí jsou společné rizikové faktory zmíněných onemocnění či zda lze nalézt společné patofyziologické rysy.
Rizikové faktory některých žilních a arteriálních nemocí se vzájemně prolínají, jak lze demonstrovat na výčtu rizikových faktorů chronického žilního onemocnění (chronic venous disease – CVD), žilní TEN a aterosklerózy (AS).
- Rizikové faktory CVD: dlouhodobá statická zátěž, nedostatek pohybu, těsný oděv, vysoké podpatky, kouření, obezita, zvýšený abdominální tlak (sedavé zaměstnání, obstipace), hormonální antikoncepce, multiparita, pozitivní rodinná anamnéza CVD, TEN v osobní anamnéze.
- Rizikové faktory žilní TEN: vyšší věk, operace, úraz, malignita, akutní interní onemocnění, imobilizace, gravidita, hormonální antikoncepce či hormonální substituční léčba, kouření, trombofilní stavy, varixy.
- Rizikové faktory AS: dyslipidemie, kouření, arteriální hypertenze, diabetes mellitus, obezita, pozitivní rodinná anamnéza komplikací AS, vyšší věk, mužské pohlaví, nedostatek pohybu, spánková apnoe, stres, nezdravá strava, nadměrný příjem alkoholu.
Etiopatogeneze CVD i AS je poměrně složitá, lze však vysledovat společné patofyziologické mechanizmy. V obou případech se uplatňuje porucha proudění krve, respektive působení abnormálního smykového napětí na cévní stěnu, zejména endotel, s navozením prozánětlivého a protrombotického fenotypu. Dochází k expresi zánětlivých cytokinů, adhezivních faktorů, interakci endotelů a leukocytů. Zánětlivý proces vede k dysfunkci či poškození endotelu v obou řečištích, a hraje tedy zásadní roli při vzniku i progresi tepenných i žilních onemocnění. Existuje řada výzkumných prací dokumentujících zvýšené hladiny určitých působků jak u žilních onemocnění (CVD, TEN), tak AS a kardiovaskulárních chorob (ICHS, CMP, ICHDK, fibrilace síní, srdeční selhání). Jedná se o ukazatele zánětu, markery aktivace leukocytů a endotelií, adhezní molekuly, chemokiny, markery aktivace koagulace či poruchy fibrinolýzy, modulátory angiogeneze, ukazatele oxidačního stresu.
Chronická žilní insuficience a kardiovaskulární onemocnění
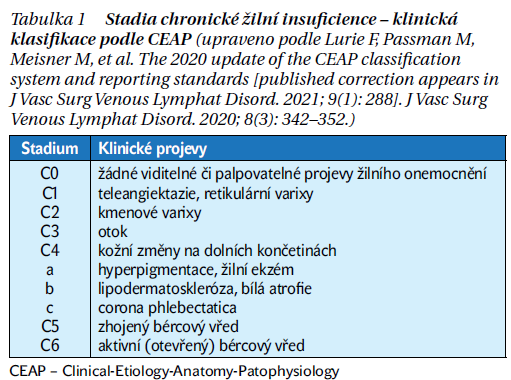
Nedávno byly publikovány výsledky velké studie dokumentující souvislost chronické žilní insuficience (chronic venous insufficiency – CVI) a kardiovaskulárních chorob, tzv. Gutenberg Health Study. Jednalo se o populační prospektivní jednocentrovou studii. Byla provedena v Německu a sledovala v letech 2012–2017 celkem 12 423 jedinců ve věkovém rozmezí 40–80 let. Na začátku studie bylo u všech účastníků provedeno klinické a laboratorní vyšetření, zjištěn výskyt kardiovaskulárních rizikových faktorů a komorbidit a zhodnocena přítomnost a stadium žilního onemocnění (CVD), respektive známky žilní insuficience (CVI). Klinická stadia CVD (C0–C6) podle tzv. CEAP klasifikace uvádí tabulka 1. Stadia C3–C6 (tedy otok, kožní změny a bércový vřed žilního původu) byla klasifikována jako CVI. Autoři studie dále kategorizovali CVI jako mírnou (C3) či pokročilou (C4–C6).
Do skupiny sledovaných kardiovaskulárních komorbidit byly zařazeny: fibrilace síní, městnavé srdeční selhání, ICHS, ICHDK, CMP a žilní TEN.
Výsledky Gutenberg Health Study
Prevalence CVD obecně byla značná – stadium C1 (teleangiektazie, retikulární varixy) bylo zjištěno u 36,5 % účastníků, stadium C2 (kmenové varixy) u 13,3 % a CVI (C3–C6) u 40,8 %. Multivariantní analýzou byly jako nezávislé prediktory všech stadií CVI prokázány vyšší věk a ženské pohlaví. CVI byla nezávisle asociována s vyšší prevalencí arteriální hypertenze, obezity, kouření a kardiovaskulárních onemocnění. Pokročilá CVI (C4–C6) pak byla významně spojena s výskytem ICHDK a žilní TEN.
Autoři se zaměřili na souvislost CVI a kardiovaskulárních onemocnění. V multivariantní regresní analýze, po adjustaci na věk, pohlaví a tradiční kardiovaskulární rizikové faktory, byla CVI nezávisle asociována s přítomností manifestního kardiovaskulárního onemocnění (prevalence zvýšena 1,46×; 95% konfidenční interval CI 1,16–1,84), přičemž tato asociace narůstala proporcionálně se stupněm CVI.
Dalším sledovaným parametrem byla mortalita ze všech příčin. Během follow-up po dobu průměrně 6,4 roku došlo k 540 úmrtím. Mortalita ze všech příčin byla významně zvýšena ve skupině s CVI. Statistická analýza s adjustací na tradiční kardiovaskulární rizikové faktory, kardiovaskulární onemocnění, onkologická onemocnění a na kardiovaskulární medikaci potvrdila CVI jako nezávislý prediktor mortality ze všech příčin (poměr rizik, hazard ratio, HR 1,46, 95% CI 1,19–1,79).
Toto zásadní zjištění, tedy zvýšení mortality ze všech příčin u jedinců s CVI, bylo ještě autory externě validováno v jiné studii – MyoVasc Study, velké prospektivní kohortové studii nemocných se srdečním selháním. V té byla u podskupiny 2 423 účastníků rovněž zhodnocena přítomnost CVI (podle klasifikace CEAP). Během sledování o průměrném trvání 3,2 roku došlo k 205 úmrtím. Statistická analýza (s adjustací na věk, pohlaví, tradiční kardiovaskulární rizikové faktory, malignitu, hodnotu N-terminálního prohormonu natriuretického peptidu B a kardiovaskulární medikaci) rovněž prokázala CVI jako nezávislý prediktor mortality ze všech příčin (HR 1,48; 95% CI 1,12–1,96).
Asociace žilních a tepenných onemocnění – podněty pro výzkum i klinickou praxi
Odhalené souvislosti si jistě zaslouží další hlubší zkoumání, ať již epidemiologické studie či výzkum zaměřený na bližší objasnění společných patofyziologických dějů nebo na vývoj a ověření nových terapeutických přístupů.
Zajímavé jsou výsledky nedávno publikované práce tchaiwanských autorů. Ti v předchozí velké retrospektivní kohortové studii (výše uvedené) dokumentovali společný výskyt varixů, ICHDK a žilní TEN. V další retrospektivní studii prokázali, že terapeutický zásah v žilním systému může mít příznivý dopad i na systém tepenný. Porovnali výskyt ICHDK a TEN ve skupině 1 323 pacientů, kteří podstoupili v letech 2005–2016 endovaskulární léčbu varixů (termální ablaci), oproti skupině 149 586 pacientů s varixy, kteří eliminační léčbu varixů nepodstoupili. Doba sledování byla do první příhody (žilní TEN či ICHDK) nebo po celou dobu studie. U pacientů po endovaskulární léčbě varixů byl statisticky významně (při použití logistické regrese s adjustací na možné rizikové faktory sledovaných komplikací) snížen výskyt nejen žilní TEN (HR 0,49; 95% CI 0,32–0,75), ale také ICHDK (HR 0,64; 95% CI 0,49–0,85).
V klinické praxi je třeba uplatňovat komplexní přístup k pacientům s cévním onemocněním, tedy např. u nemocného přicházejícího do ordinace pro příznaky CVI se zaměřit i na možné rizikové faktory, případně již přítomné známky kardiovaskulárního onemocnění a provést v tomto směru pečlivé klinické, případně i přístrojové vyšetření. V primární i sekundární prevenci je třeba snažit se monitorovat a ovlivňovat rizikové faktory žilních i tepenných onemocnění, případně léčit již subklinické formy těchto nemocí. Tématem pro praxi i výzkum je použití léčby zasahující patofyziologické mechanizmy v tepenném i žilním řečišti. Potenciální léčebné strategie by se měly zaměřit na protizánětlivé působení, úpravu endoteliální dysfunkce, zlepšení hemoreologických parametrů, ovlivnění prokoagulačního stavu i negativních metabolických vlivů.
Závěr
Epidemiologické studie, základní a klinický výzkum i zkušenosti z praxe potvrzují souvislost mezi žilními a tepennými chorobami. Ačkoli se ve svých ambulancích zabýváme obvykle jen jednou stránkou cévního řečiště, nelze oba systémy vnímat odděleně. Při onemocnění žil a tepen se uplatňují podobné patofyziologické děje (porucha krevního proudění, chronické zánětlivé procesy, dysfunkce a poškození endotelu). Přístup k cévnímu pacientovi tedy má být komplexní se snahou o ovlivnění rizikových faktorů a zachycení časných fází onemocnění.
doc. MUDr. Jana Hirmerová, Ph.D.
II. interní klinika LF UK a FN Plzeň
