Bronchogenní karcinom, který obvykle souvisí s letitým kuřáctvím, je v naší populaci malignitou s vysokou incidencí a bohužel i mortalitou. Incidence v ČR z roku 2018 dokládá čísla 60,8/100 000 obyvatel, mortalita přestavuje 49,1/100 000 obyvatel. Přestože byl v posledním desetiletí zaznamenán v oblasti pneumoonkologie vysoký léčebný posun, stále nás čeká ještě dlouhá cesta, abychom tuto zákeřnou chorobu mohli nazvat „chronickým onemocněním“.
Kam jsme se posunuli v léčbě pokročilých stadií?
Přes 20 let byla jedinou léčebnou možností pro nemocné s malobuněčným karcinomem plic chemoterapie na bázi platinového derivátu s etoposidem a radioterapie. Rok 2022 se stal zlomovým, neboť v současné době je nadosah imunoterapie (atezolizumab, durvalumab) a v nejbližších týdnech se očekává i úhrada zdravotními pojišťovnami pro extenzivní formu této nemoci.
U nemalobuněčného karcinomu plic jsou stále vidět pokroky, rok co rok. U lokalizované formy nemoci (stadium III) a generalizované (stadium IV) je dnes již standardem testování řídicích mutací (reflexně EGFR, ALK ROS1) a PD-L1, které je prediktorem úspěšnosti imunoterapie.
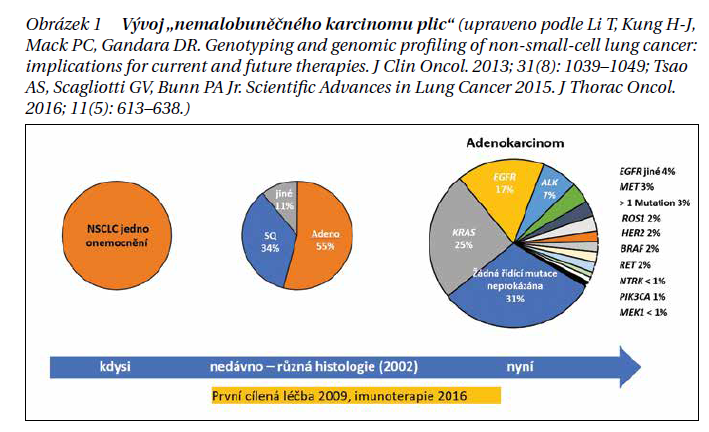
Stále častěji je indikováno i testování pomocí NGS (next generation sekvenování) k zachycení dalších, vzácnějších mutací, na které již existuje cílená léčba, i když dosáhnout na ni je obtížnější a je třeba žádat schválení příslušné zdravotní pojišťovny. K tomu byly ustanoveny tzv. tumor boardy, kdy tým expertů indikuje vyšetření NGS s cílem zvýšit u nemocných záchyt mutací, a terapeuticky tak zacílit léčbu. Pro nemocné s mutací EGFR nyní máme k dispozici tyrosinkinázové inhibitory II. a III. generace (gefitinib, erlotinib, afatinib, osimertinib, dakomitinib), pro nemocné s translokací ALK jsou indikovány cílené preparáty brigatinib, alektinib, lorlatinib, krizotinib a ceritinib. V případě ROS1 pozitivních nemocných je indikován entrektinib či krizotinib, u BRAF pozitivních dabrefenib, u nemocných s NTRK 1, 2, 3 je možnost léčby entrektinibem či larotrektinibem, u nemocných s mutací RET zase selperkatinib či pralsetinib, u MET tepotinib či u KRAS mutace subtypu G12C sotorasib (obrázek 1).
Jak již bylo zmíněno, dnes je standardem testování exprese PD-L1 u nemocných s nemalobuněčným plicním karcinomem (NSCLC). Jde o zatím nejslibnější a v praxi realizovatelný prediktor úspěšnosti imunoterapie. V minulých letech byla indikací k imunoterapii hodnota nad 50 %, v létě roku 2020 získal pembrolizumab v kombinaci s chemoterapií úhradu do první linie léčby u nemocných s expresí 1–49 %. Na konci roku 2021 pak byla schválena úhrada pro pacienty i s nulovou expresí PD-L1, a to kombinací nivolumab + ipilimumab (+ chemoterapie).
K říjnu 2022 tak máme k dispozici pro pacienty s lokálně pokročilým a generalizovaným onemocněním celý arzenál léčiv z řady tzv. checkpoint inhibitorů, anti-PD1 (atezolizumab, durvalumab), anti-PD-L1 (nivolumab, pembrolizumab, cemiplimab) a anti-CTLA4 (ipilimumab). Trend je posouvat tato léčiva do první linie léčby, pokud nemocný splní indikační kritéria.
Co nás v této chvíli ale trápí, je stále limitovaná absence širšího spektra prediktivních biomarkerů a imunomarkerů. Slibně zatím vypadají výsledky prediktivní analýzy mikrobiomu, kdy předběžné výsledky prokázaly, že střevní mikrobiom může výrazně determinovat účinnost protinádorové imunity, a modulace mikrobiomu je dokonce jednou z nových možností, jak zvýšit účinnost imunoterapie.
Pokrok u kurativních stadií karcinomu plic
Pro nemocné s nízkými stadii nemoci I–IIIA byla donedávna standardem radikální operace a s ohledem na zvážení rizikovosti rekurence a komorbidit pak následná adjuvantní léčba chemoterapií či radioterapií. Pokud byl nemocný kontraindikován k chirurgickému výkonu (nejčastěji pro interní komorbidity a pro funkční ventilační limitace), nahrazovala operaci radikální radioterapie. Tyto principy se nijak zásadně nezměnily ani dnes, naopak došlo k rozšíření adjuvantních možností.
Pokud je v biopsii prokázána EGFR mutace (což bývá především u nekuřáků), lze zvážit i adjuvantní cílenou léčbu osimertinibem. V očekávání je i adjuvantní imunoterapie, která již prokázala v řadě studií svůj benefit.
Zavedení screeningu
Rok 2022 se stal zlomovým i co se týká spuštění screeningu karcinomu plic. Je určen pro nemocné ve věkové kategorii 55–74 let, tedy nejrizikovější věkové skupiny, kteří kouřili cca 20 let 20 cigaret denně nebo s adekvátním zatížením (např. 10 let/40 cigaret/den). Do tohoto programu jsou zařazeni i nemocní, kteří již přestali kouřit, ale kuřáctví mají v anamnéze. Pacienti absolvují nízkodávkové (low dose) CT vyšetření spolu s protikuřáckou intervencí. Očekáváním je podle výsledků studií v Evropě i USA včasný záchyt nízkých (bezpříznakových) stadií nemoci a s tím i výrazné snížení mortality na toto onemocnění (až o 20–25 %).
Radioterapie bronchogenního karcinomu
I na poli radioterapie došlo pro pacienty s bronchogenním karcinomem k pokroku a spolupráce s radiačními onkology je klíčová v boji za delší přežití. Pokročilé techniky radioterapie, jakou jsou IMRT (intensity modulated radiotherapy) a IGRT (image guided radiotherapy) se zohledněním dýchacích pohybů umožňují redukovat dávku na srdce a zdravou plíci, a snižují tak riziko poradiační pneumonitidy, která je zvláště u těchto nemocných, letitých kuřáků s často přidruženou CHOPN dost limitující na kvalitě života.
Volit lze nejen fotonové záření, ale i protonové. U tumorů menší velikosti, kdy pacient je kontraindikován k chirurgickému výkonu a kdy je cílem podání radikální dávka, bylo zaznamenáno výrazně vyšší využití metody Cyberknife, a to právě z důvodu šetrnosti k okolní plicní tkáni. I zde platí, že vhodnou metodu pro daného nemocného navrhuje specializovaný tým s radioterapeuty v čele.
Budoucnost léčby karcinomu plic
Pokud se ohlédneme např. 10 let zpět, vidíme obrovský posun v léčbě plicních nádorů. Troufám si říct, že pneumoonkologie dosáhla jednoho z největších rozmachů v klinické onkologii. Trend, kterým se ubíráme, směřuje k personalizované a precizní medicíně. Už nyní je pryč éra, kdy terapie byla určena na základě histologického vyšetření a všichni nemocní s touto diagnózou a stadiem choroby měli stejnou léčbu. Nově bude (částečně již je) každému nemocnému na základě zjištěných molekulárních indikátorů, informací o tumoru, pacientovi a jeho preferencích indikována „léčba na míru“.
Závěr
Již nyní jsou výrazné pokroky v délce přežití nemocných, aniž by docházelo ke zhoršení jejich kvality života. Není výjimkou, že se nemocní dožívají několika let i při vstupně diagnostikovaném pokročilém onemocnění.
V závěru je třeba zmínit pokrok také v nelékařské oblasti, především u pacientských organizací a v informovanosti veřejnosti o tomto onemocnění, které se může týkat kohokoli z nás (i nekuřáků!) či z našeho okolí.
Práce byla podpořena výzkumným programem Univerzity Karlovy Cooperatio 34 – Vnitřní obory.
MUDr. Jana Krejčí
Plicní klinika 3. LF UK a FN Bulovka, Praha
