Až u 25 % pacientek s HR-pozitivním a HER2-negativním karcinomem prsu dojde k relapsu onemocnění. Metastatické onemocnění je i nadále nevyléčitelné. Základní léčebnou modalitou je hormonální léčba, ovšem u všech pacientek dochází ke vzniku hormonální rezistence. Snahou o překonání nebo oddálení této rezistence je kombinovaná léčba – kombinace hormonální léčby s léčbou cílenou. Průlomem v terapii jsou inhibitory CDK 4/6, které jsou kombinovány s nesteroidním inhibitorem aromatáz nebo fulvestrantem. Z dalších cílených preparátů se blíží použití do klinické praxe (jsou schváleny EMA, ale doposud nemají v ČR úhradu) alpelisib a pro pacientky se zárodečnou mutací v genech BRCA1/2 jsou to inhibitory PARP.
Karcinom prsu s expresí hormonálních receptorů (HR+) a negativitou receptoru pro lidský epidermální růstový faktor 2 (HER2–; human epidermal growth factor receptor 2) je nejčastěji se vyskytující podtyp. Až 75 % žen s karcinomem prsu má nádor prsu exprimující estrogenový receptor (ER) a/nebo progesteronový receptor (PR). Hormonální terapie (HT) je nejstarší cílenou onkologickou léčbou. Adjuvantní hormonální léčba je pro většinu žen s pozitivitou HR vysoce účinná. I přes existující adjuvantní systémovou cílenou terapii dochází asi u třetiny z nich k progresi onemocnění. Metastatický karcinom prsu zůstává i nadále nevyléčitelným onemocněním, 5 let se vzdálenými metastázami přežívá kolem 25 – 30 % pacientek. Preferovanou terapií je u metastatického HR+/HER2– karcinomu prsu v posledních letech hormonální léčba. Účinnost HT je bohužel limitována existencí primární nebo vznikem sekundární hormonorezistence. Volba 1. linie pro postmenopauzální pacientky závisí na předchozím typu adjuvantní HT, její délce a případně době od ukončení adjuvantní HT. Můžeme volit mezi inhibitorem aromatáz, tamoxifenem nebo fulvestrantem.
V současné době je preferovanou léčebnou možností kombinace hormonální terapie s inhibitorem CDK 4/6. V dnešních dnech máme k dispozici tři – palbociklib, ribociklib a abemaciklib. Léčebnou možností je kombinace NAI (nesteroidního inhibitoru aromatáz) nebo fulvestrantu s inhibitorem CDK 4/6 – palbociklibem, ribociklibem nebo abemaciklibem. Přidání inhibitoru CDK 4/6 k NAI vedlo v 1. linii k téměř dvojnásobnému prodloužení doby do progrese onemocnění (PFS – progression-free survival) v porovnání s monoterapií NAI; jedná se zhruba o 13 – 15 měsíců. U pacientek po selhání NAI dochází v kombinaci s fulvestrantem k prodloužení PFS o 5 – 7 měsíců v porovnání s léčbou samotným fulvestrantem.
Ve čtyřech studiích fáze III byly již publikovány konečné údaje celkového přežití (OS – overall survival). Studie PALOMA 3 – kombinace palbociklibu s fulvestrantem – prokázala prodloužení OS o 6,9 měsíců v porovnání s fulvestrantem samotným. Studie MONARCH 2 (kombinace abemaciklibu s fulvestrantem), studie MONALEESA 3 (kombinace ribociklibu s fulvestrantem) a studie MONALEESA 7 (kombinace ribociklibu s NAI u premenopauzálních pacientek) prokázaly statisticky signifikantní prodloužení OS u pacientek léčených kombinační terapií se snížením rizika úmrtí o 28 – 29 % u ribociklibu a o 24 % u abemaciklibu (viz tabulka 1).
Toxicita všech tří inhibitorů CDK 4/6 je porovnatelná. Nejčastějšími nežádoucími účinky (NÚ) jsou neutropenie, leukopenie, anemie, únava, nevolnost, zvracení a zvýšení jaterních testů. Pouze u abemaciclibu je vyšší výskyt průjmů. Všechny NÚ jsou většinou velmi dobře léčebně ovlivnitelné.
Klinické studie s alpelisibem
Novým cíleným preparátem, který prokázal přínos v kombinaci s hormonální léčbou u metastatického HR+ karcinomu prsu po předchozím selhání NIA je alpelisib. Jedná se o selektivní alfa-specifický inhibitor PI3K, který prokázal účinnost u nádorů s mutací v genu PIK3CA. Mutace se vyskytuje u nádorů HR+/HER2– až ve 40 % a její přítomnost je spojena s horší prognózou. V randomizované klinické studii fáze III SOLAR-1 byl porovnáván alpelisib + fulvestrant s placebem + fulvestrantem u pacientek s pokročilým karcinomem prsu HR+/HER2–, které byly předtím léčeny hormonoterapií. Ve skupině pacientek s nádorovou mutací v PIK3CA byla prokázána signifikantně delší PFS ve 20měsíčním sledování. Ve skupině léčené kombinací alpelisib+ fulvestrant byla pozorována dvojnásobná PFS – 11 měsíců v porovnání s 5,7 měsíci ve skupině léčené pouze fulvestrantem (HR: 0,65; 95% CI: 0,50 – 0,85; P ˂0,001). Účinná byla terapie u pacientek bez ohledu na linii léčby a i u předtím již léčených inhibitorem CDK 4/6, kterých bylo ale minimum (5,6 %). S ohledem na současné léčebné standardy, kterými je zařazení inhibitoru CDK 4/6 v úvodu terapie pro metastatické onemocnění, byla navržena klinická studie BYLive, kam byly zařazovány pacientky již předtím léčené inhibitorem CDK4/6. Byl potvrzen primární sledovaný ukazatel – 50,4 % pacientek bylo bez progrese onemocnění po dobu minimálně 6 měsíců. Byla tedy prokázána účinnost alpelisibu po předchozí terapii s inhibitory CDK 4/6. Nejčastějšími nežádoucími účinky stuoně 3 a 4 byly hyperglykemie, rash a průjmy.
Obrázek 1 Mechanismus účinku inhibitorů CDK 4/6
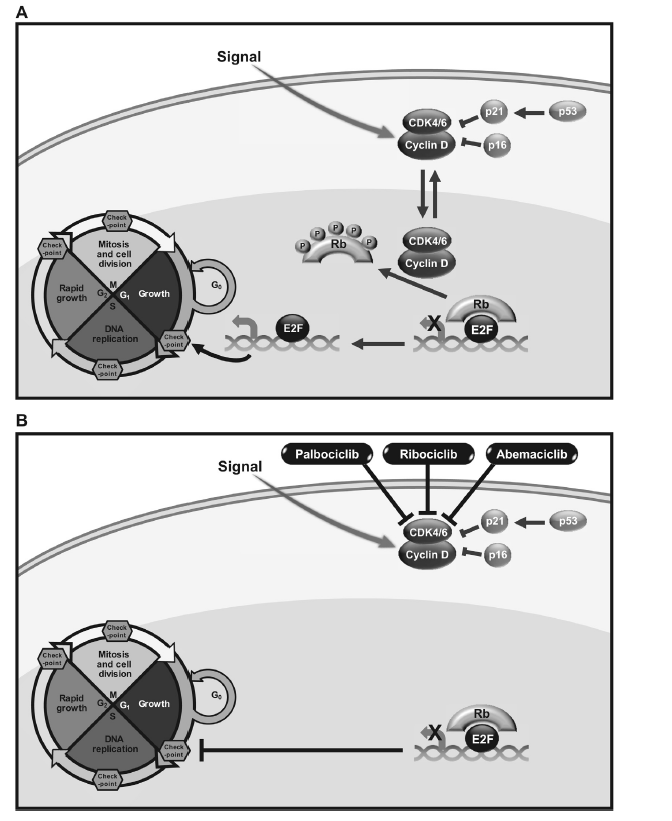
Podle E. Hamiltona, 2016.
A – dráha cyklin D – CDK 4/6 – Rb
B – inhibice CDK 4/6 způsobí pokles koncentrace fosforylovaného komplexu Rb a Rb-E2F a zabrání tím aktivitě retranskripčního faktoru E2F, čímž zabrání přesunu buněčného cyklu z fáze G0 do fáze G1.
Inhibitory PARP – olaparib, talazoparib
Pro úzce specifikovanou skupinu pacientek nejenom s HR+ a HER2–karcinomem prsu není možno opominout léčebnou skupinu inhibitorů PARP – olaparib a talazoparib. Jedná se o skupinu pacientek s prokázanou germinální mutací v genech BRCA1 a BRCA2. Poly-(ADP-ribózo) polymerázy (PARP) hrají zásadní roli při opravě poškozené DNA – viz obrázek 2. Proto je možné je využít v léčbě karcinomu prsu spojeného s germinální mutací v genech BRCA1/2. Geny BRCA1 a BRCA2 jsou reparační geny a při jejich mutaci dochází k poruše opravy DNA, což způsobuje vyšší výskyt určitých malignit (především nádorů prsu a ovarií). Nicméně tohoto „nedostatku“ je možno využít v terapii nádorů prsu, neboť tyto nádory jsou více citlivé na preparáty, které působí poškození DNA.
Obrázek 2 Role PARP při opravě jednovláknových zlomů DNA
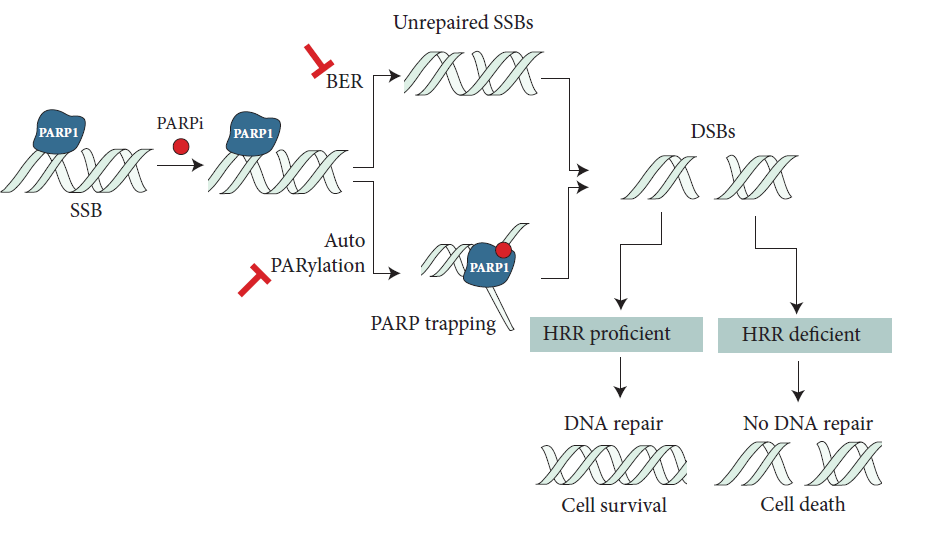
Podle J. Mateo, Annals of Oncol. 2019.
Olaparib byl zařazen do klinické praxe na základě výsledků registrační studie fáze III OlympiAD. Do této studie byly zařazeny pacientky s metastatickým karcinomem prsu, které byly randomizovány do větve s olaparibem nebo do větve s chemoterapií podle výběru onkologa. Studie splnila svůj cíl – prokázala zlepšení v parametru PFS v porovnání s chemoterapií. V hodnocení celkového přežití byl prokázán největší účinek ve větvi s olaparibem u pacientek, které nebyly předtím léčeny chemoterapií pro metastatické onemocnění v porovnání s kontrolní větví (22,6 vs. 14,7 měsíců).
Dalším z inhibitorů PARP je talazoparib, u něhož byla také prokázána účinnost u metastatického karcinomu prsu u pacientek s mutací BRCA1/2.V podobně uspořádané studii fáze III EMBRACA byla porovnávána účinnost talazoparibu s terapií podle volby lékaře.). I v této studii byl prokázán účinek v PFS; talazoparib signifikantně prodloužil PFS – 8,6 měsíců vs. 5,6 měsíců (HR 0,542; P <0,001). Léčba inhibitory PARP je podle výsledků obou uvedených studií nejenom účinná, ale i bezpečná a je spojena s velmi dobrou kvalitou života.
Kombinovaná léčba – hormonální léčba s everolimem a exemestanem
I nadále využíváme v klinické praxi osvědčenou kombinaci hormonální léčby s everolimem. Everolimus je inhibitor mTOR, jenž ovlivňuje intracelulární dráhu PI3K, která je často hyperaktivována právě u tohoto podtypu karcinomu prsu. Aktivace této dráhy je popisována jako jeden z mechanismů hormonální rezistence. Everolimus se používá u pacientek s metastatickým karcinomem prsu, které absolvovaly již předchozí hormonální léčbu pro metastatické onemocnění. Podáván je v kombinaci s exemestanem na základě registrační studie BOLERO 2. Ve studii BOLERO 2 bylo prokázáno prodloužení PFS ve větvi s kombinací exemestan + everolimus proti monoterapii s exemestanem na dvojnásobek. Konečné údaje byly publikovány po 18 měsících sledování a prokázaly rozdíl 6,9 měsíců v PFS – 11,0 měsíců pro kombinaci versus 4,1 měsíce ve skupině s monoterapií exemestanem (HR 0,38; 95% CI: 0,31 – 0,48; P ˂0,0001). Tuto léčebnou variantu je možno nabídnout pacientkám po předchozím léčení hormonální monoterapií, popř. kombinací s inhibitorem CDK 4/6 u metastatického onemocnění. Z nejčastěji se vyskytujících nežádoucích účinků je popisována stomatitida, intersticiální pneumonitida, kožní enantém, únava a hyperglykemie (viz obrázek 3).
Obrázek 3 Signální dráhy vedoucí u karcinomu prsu k růstu a přežití.
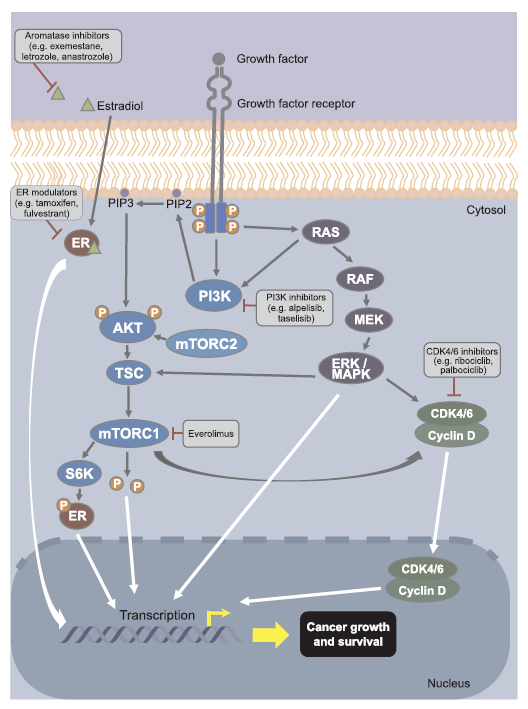
Zdroj: archiv autorky
Léčebná doporučení u premenopauzálních pacientek
Je potřeba zmínit ještě zásadní informaci. Všechna uvedené údaje platí pro postmenopauzální pacientky. Přestože je karcinom prsu nádorem žen staršího věku, vyskytuje se i u žen premenopauzálních. Léčebná doporučení pro premenopauzální pacientky jsou extrapolována ze studií pro pacientky postmenopauzální. Neboť prvním krokem u metastatického HR+/HER2– karcinomu prsu by mělo být provedení ovariální ablace. Je možno použít všechny 3 metody – tzn. chirurgickou, radiační nebo chemickou pomocí LH-RH analog. Tímto se stane pacientka ženou postmenopauzální, a proto je využíváno údajů z klinických studií pro postmenopauzální pacientky, ač donedávna nebyly k dispozici žádné klinické studie speciálně uspořádané pro premenopauzální pacientky. Speciálně uspořádanou multicentrickou klinickou studií fáze III pro premenopauzální pacientky byla studie MONALEESA 7. Léčeny byly pacientky s HR+/HER2– pokročilým karcinomem prsu, které byly randomizovány do kombinační větve s ribociklibem versus větve s placebem. Z hormonální léčby mohly být léčeny tamoxifenem nebo inhibitorem aromatáz vždy s goserelinem. Potvrzen byl účinek z předchozích studií postmenopauzálních pacientek. Došlo k prodloužení PFS o 10,8 měsíců ve větvi s kombinací v porovnání s placebem.
Závěr
V současné době zatím neznáme optimální sekvenci jednotlivých léčebných kombinací, popř. monoterapie u pacientek s pokročilým HR+/HER2– karcinomem prsu. Přesto však i přes zatím spoustu ještě nezodpovězených otázek se staly inhibitory CDK 4/6 jedním ze zásadních průlomů v léčbě luminálního metastatického karcinomu prsu. Preferovanou léčebnou variantou u HR+/HER2– metastatického karcinomu prsu je v 1. linii kombinace HT s inhibitorem CDK 4/6, dalšími variantami je možná pouze hormonální léčba monoterapií. Volba léčebné varianty závisí na předchozí terapii, toxicitě léčby, délce bezpříznakového období, rozsahu onemocnění, závažných interkurencích, biologickém věku, výkonnostním stavu (PS) a samozřejmě v neposlední řadě i na preferencích pacientky.
V dalších liniích je možno využít kombinace fulvestrantu s inhibitorem CDK 4/6, kombinace everolimus + exemestan, snad brzy i kombinace fulvestrantu s alpelisibem u pacientek s prokázanou mutací PIK3CA. Další z možností pro pacientky s prokázanou zárodečnou mutací v genech BRCA1/2 je monoterapie inhibitorem PARP. Dlouhodobým cílem v onkologii nejenom u karcinomu prsu je snaha „ušít pacientkám terapii co nejvíce na míru“. Určitě existuje skupina pacientek, jimž můžeme v 1. linii pro metastatické onemocnění nabídnout pouze monoterapii s výborným účinkem a kombinovanou léčbu zvolit až v dalších liniích. Problémem zůstává znalost specifických markerů, na jejichž základě bychom se rozhodovali. Toto nám doposud v klinické praxi chybí. Cílem této personalizované terapie je snaha nejenom o vyšší účinnost léčby, ale i o nižší toxicitu onkologické léčba a její ekonomickou náročnost. Zatím pouze v rámci výzkumných projektů je možno provádět genetické testování buď z tkáně, nebo ze séra, a právě na základě zjištěných mutací je možno očekávat do budoucna volbu léčebné kombinace.
MUDr. Markéta Palácová
Klinika komplexní onkologické péče
Masarykův onkologický ústav, Brno
