Již XXVIII. západočeské pneumoonkologické dny se letos uskutečnily ve dnech 9.–11. listopadu v kongresovém centru Parkhotelu v Plzni. Ve čtvrtek dopoledne vystoupila čtveřice specialistů v bloku zdůrazňujícím přínos multidisciplinárního přístupu v léčbě karcinomu plic.
V ČR je ročně diagnostikováno přes 6 500 případů karcinomu plic, přičemž 20 % nemocných je v době diagnózy ve stadiu III, které je velmi heterogenní a představuje nádory různé velikosti a s různým postižením uzlin. Většina pacientů stadia III má neresekabilní onemocnění, léčbou volby je chemoradioterapie (CRT), prognóza je ale nepříznivá.
Osimertinib v terapii EGFRm NSCLC
Jako první se ujal slova MUDr. Martin Svatoň, Ph.D., který se ve své přednášce věnoval inhibitoru tyrozinkinázy (TKI) – osimertinibu – v adjuvantní terapii. Osimertinib je ireverzibilním inhibitorem receptoru epidermálního růstového faktoru (EGFR) s aktivačními mutacemi (EGFRm) a mutací T790M rezistentní k TKI. EGFR se podílí na růstu a dělení buněk, aktivační mutace tohoto receptoru vede k nadměrnému a nekontrolovanému růstu a proliferaci nádorových buněk.
Studie ADAURA
Adjuvantní, placebem kontrolovaná (1 : 1) studie ADAURA zkoumala vliv terapie osimertinibem u resekovaných pacientů ve stadiu IB–IIIA (n = 682) zařazených nezávisle na předchozí adjuvantní chemoterapii. Pacienti podstoupili radikální resekci včetně disekce lymfatických uzlin a před randomizací podstoupili CT trupu a CT nebo MRI mozku, podmínkou byla absence neoadjuvantní chemoterapie a radioterapie. Pacienti byli stratifikováni podle výskytu mutace s delecí exonu 19 receptoru EGFR nebo substituční mutací exonu 21 (L858R). Užívali 80 mg osimertinibu denně a plánovaná délka léčby byla 3 roky. Odslepení výsledků předběžné analýzy o 2 roky dříve bylo doporučeno nezávislou komisí pro kontrolu dat s ohledem na zřejmou velikost léčebného přínosu; nicméně zkoušející lékaři i pacienti, kteří pokračovali ve studii, zůstali z hlediska podávané léčby zaslepeni.
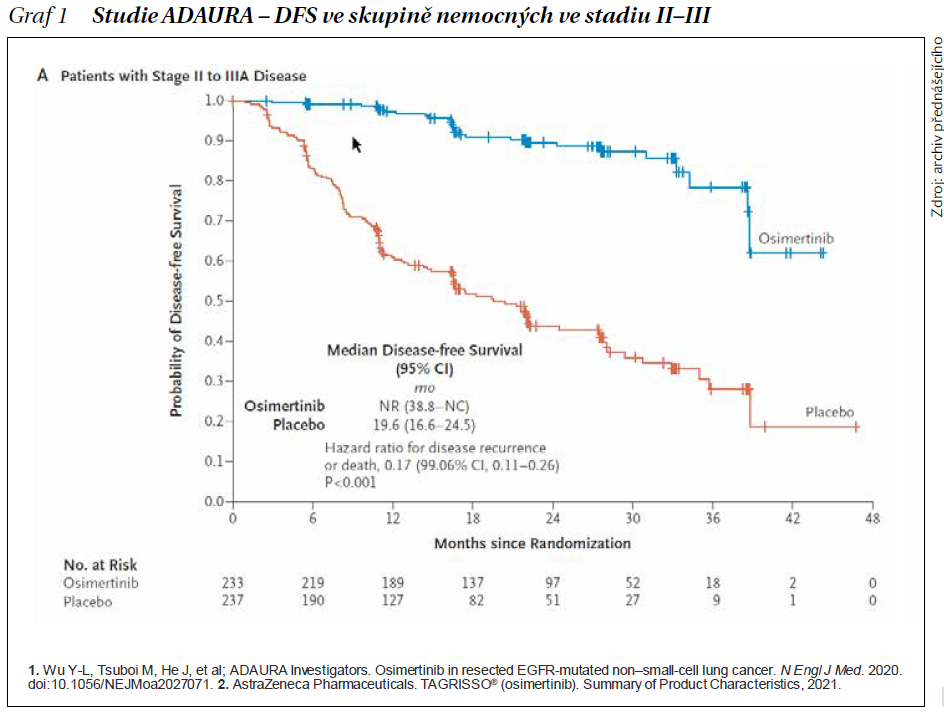
Primárním cílem studie bylo přežití bez známek onemocnění (DFS) u pacientů s NSCLC stadií II a IIIA, který byl naplněn se signifikantním benefitem pro pacienty. mDFS nebylo v průběhu studie dosaženo (HR = 0,17 (99,06 % CI: 0,11–0,26), což představuje impozantní 83% redukci rizika rekurence onemocnění nebo úmrtí (graf 1). Nové léze byly v rameni s osimertinibem méně často pozorovány v lokálních, a především distálních regionech. Obdobný signifikantní benefit DFS byl pozorován také pro pacienty ve stadiu IB–IIIA (HR = 0,20, 99,12 % CI: 0,14–0,30).
Indikace osimertinibu
Osimertinib je indikován k adjuvantní léčbě po úplné resekci nádoru u dospělých pacientů s nemalobuněčným karcinomem plic (NSCLC) ve stadiu IB–IIIA, jejichž nádory mají delece exonu 19 receptoru epidermálního růstového faktoru (EGFR) nebo substituční mutaci exonu 21 (L858R), k léčbě první linie dospělých pacientů s lokálně pokročilým nebo metastazujícím NSCLC s aktivačními mutacemi EGFR a k léčbě dospělých pacientů s lokálně pokročilým nebo metastazujícím NSCLC s přítomnou mutací EGFR T790M.
Radioterapie lokálně pokročilého NSCLC
MUDr. Radovan Vojtíšek, Ph.D., úvodem vzpomenul historii radioterapie a studii publikovanou v roce 2011, která ustanovila normofrakcionovanou konkomitantní radiochemoterapii (60 Gy) jako standard léčby lokálně pokročilého NSCLC. Tento režim dosáhl nejdelšího mediánu celkového přežití (mOS = 17 měsíců).
Kazuistika
Prostřednictvím kazuistiky dr. Vojtíšek prezentoval benefity multidisciplinárního přístupu k terapii NSCLC a přínos adjuvantní terapie durvalumabem. 64letý pacient, kuřák, podstoupil pro hemoptýzu rtg plic (6/2020) s nálezem v pravé plíci. PET/CT vyšetření (8/2020) odhalilo přítomnost tumoru o velikosti 58 × 51 × 55 mm v S3 pravé plíce v těsném kontaktu s mediastinem a lymfadenopatií v pravém plicním hilu (24 mm) a pretracheálně (16 mm), klasifikovaného jako T3N2M0. Biopsie tumoru a cytologie pretracheální uzliny vedle k diagnostice dlaždicobuněčného karcinomu vykazující 100% expresi PD-L1.
Plánovací CT vyšetření stanovilo cílové objemy ozáření (primární tumor a pravostrannou dolní paratracheální oblast) a kritické struktury, které je snaha co nejvíce chránit (srdce, jícen, plíce, míchu). Multidisciplinární tým indikoval radikální konkomitantní radiochemoterapii primárního tumoru a vybraných uzlinových oblastí s následným adjuvantním podáváním durvalumabu, přičemž 2 cykly (vinorelbin/cisplatina) byly aplikovány před a 2 cykly v průběhu radioterapie (11–12/2020). Pacient byl ozařován normofrakciovaně (33 frakcí à 2 Gy do celkové dávky 66 Gy) technikou s objemovou modulací (VMAT), umožňující optimalizaci ozařovacího plánu.
Pět dní po zakončení radiochemoterapie potvrdilo postradiační CT hrudníku (1/2021) parciální odpověď na radioterapii – došlo k regresi tumoru o 20 % a zmenšení hilové uzliny na velikost 16 × 14 mm, načež bylo u pacienta zahájeno adjuvantní podávání durvalumabu v dávce 10 mg/kg jako intravenózní infuze po dobu 1 hodiny. Pacient je medikován ambulantně, a to ve dvoutýdenních intervalech. K listopadu 2021 bylo provedeno 17 aplikací s velmi dobrou tolerancí pacienta. V průběhu adjuvantní terapie durvalumabem dále docházelo k dalšímu zmenšování objemu nádoru. Kontrolní CT po 4 cyklech durvalumabu (3/2021) ukázalo další zmenšení o 25 %, 8/2021 pozorované jako pruhované reziduum.
Tento příklad z praxe potvrzuje účinnost radikální konkomitantní radiochemoterapie s adjuvantní imunoterapií durvalumabem.
Možnosti léčby NSCLC
Tématem příspěvku MUDr. Gabriely Krákorové, Ph.D., byl durvalumab jako konsolidační léčba po radikální chemoradioterapii (CRT) lokálně pokročilého NSCLC. Prognózy pacientů ve stadiu III nejsou příznivé, u většiny z nich dochází po radiační léčbě k relapsu. Zlepšení diagnostiky metodami PET/CT umožňuje lepší klinický staging, selektivní ozařování postižených etáží, patologický lokoregionální uzlinový staging pro přesné určení rozsahu postižení regionálních lymfatických uzlin a vyloučení vzdálených metastáz.
V posledních 10 letech došlo v systémové léčbě tohoto onemocnění pouze k omezenému pokroku a mnohé studie selhaly. Neosvědčily se indukční ani konsolidační chemoterapie, vysoké dávky RT, cílená léčba po či souběžně s RT. Také profylaktická ozáření mozku po RT neprokázala benefit.
Imunoterapie ve vztahu k radioterapii
Studie PACIFIC
V další části dr. Krákorová interpretovala výsledky robustní studie PACIFIC – první studie s adjuvantní imunoterapií durvalumabem, která u těchto pacientů přinesla benefit. Do studie byli zařazení pacienti 1–42 dní (n = 713) po úspěšné konkomitantní CRT randomizovaní v poměru 2 : 1 (durvalumab vs. placebo). Primárními cíli studie PACIFIC byly celkové přežití (OS) a doba přežití bez progrese onemocnění (PFS). V současné době jsou k dispozici aktualizované výsledky studie po 5 letech od randomizace posledního pacienta zařazeného do této studie, které potvrzují statisticky signifikantní benefit konsolidační léčby durvalumabem, významné prodloužení OS (graf 2) a PFS (graf 3) ve srovnání s placebem.
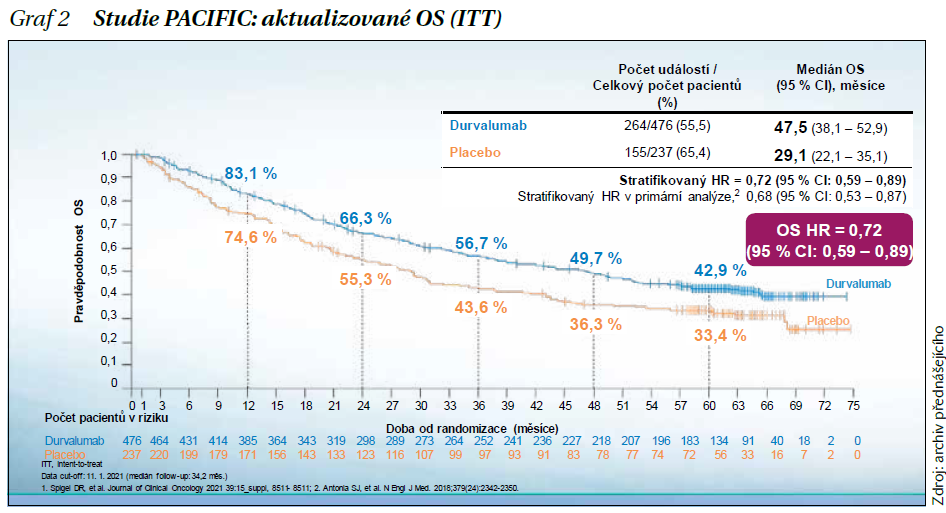
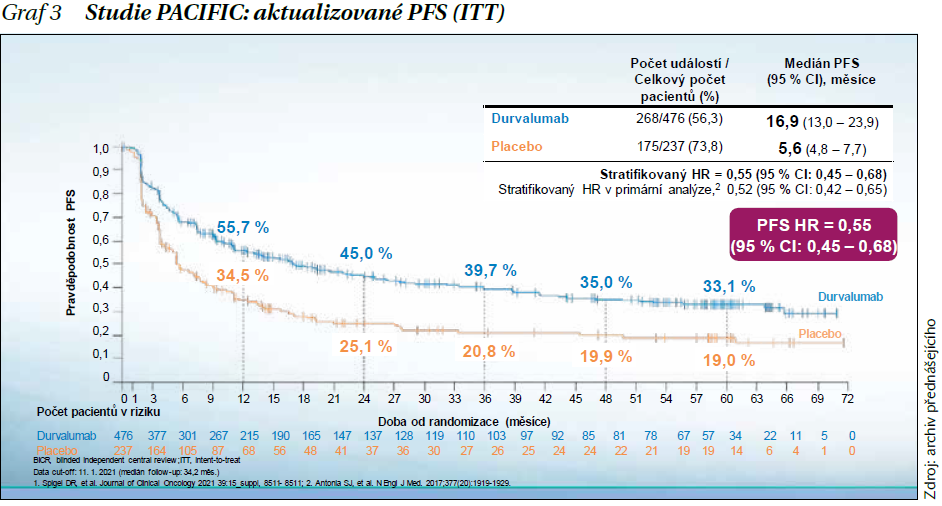
Závěry studie PACIFIC: Prodloužení OS a PFS bylo pozorováno u všech specifikovaných podskupin. U durvalumabu byl prokázán klinicky významný přínos z hlediska objektivní odpovědi na léčbu (ORR = 28,4 vs. 16,0 %, P < 0,001). V rameni s durvalumabem byl zaznamenán nižší výskyt nových lézí včetně nových metastáz v mozku. Bezpečnostní profil durvalumabu byl hodnocen jako příznivý, srovnatelný s jinými imunoterapeutiky. V průběhu studie nebyly identifikovány žádné nové bezpečnostní signály.
Imunoterapie v léčbě malobuněčného karcinomu plic
Posledním přednášejícím byl prof. MUDr. Miloš Pešek, CSc., který se detailně věnoval profilu malobuněčného karcinomu plic (SCLC) a současným možnostem terapie. SCLC je nádorové onemocnění s vysokým stupněm diferencovanosti s pozitivitou epiteliálních nebo neuroendokrinních markerů. SCLC může vznikat také histologickou transformací EGFR mutovaného adenokarcinomu. K diagnostice dochází převážně v pokročilých stadiích (70 %), přičemž hlavním rizikovým faktorem vzniku je kouření. Míra 5letého přežití je zhruba 6 %. Standardem léčebné péče v 1. linii SCLC je již téměř 20 let kombinace platinových derivátů a etoposidu, případně irinotekanu ve 4–6 cyklech.
SCLC je zpočátku chemosenzitivní – četnost odpovědí na 1. linii léčby je u limitovaného stadia (LS-SCLC) vyšší než u extenzivního stadia onemocnění (ES-SCLC). ES-SCLC je obvykle nevyléčitelný a v důsledku vysoké úmrtnosti se pouze malý počet (< 20 %) pacientů dostane až do 3. linie léčby. Klíčové charakteristiky SCLC zahrnují vysokou genomickou nestabilitu s vysokou mutační náloží, vysokou buněčnou proliferaci a růstovou kinetiku, jakož i časný vznik metastáz a chemosenzitivitu. Vysoká mutační nálož SCLC může predikovat odpověď na imunoterapii.
V posledních letech bylo provedeno několik studií s kombinací chemoterapie s imunoterapií v 1. linii. Cílem kombinování protinádorové imunoterapie je maximalizace potenciálu imunitního systému likvidovat přítomný nádor.
Studie CASPIAN
Studie CASPIAN byla randomizovaná otevřená multicentrická klinická studie u dosud neléčených pacientů s ES SCLC, kteří byli vhodní k léčbě chemoterapií na bázi platiny jako léčbě první linie pro SCLC. Do studie byli zařazeni i pacienti s asymptomatickými nebo léčenými mozkovými metastázami. Dvě stě šedesát osm pacientů bylo zařazeno do skupiny durvalumab plus platina-etoposid a 269 do skupiny platina-etoposid. Primárním cílem bylo celkové přežití (OS), dalšími sledovanými parametry byly PFS, ORR, bezpečnost a snášenlivost a kvalita života.
Přidání durvalumabu k chemoterapii významně zlepšilo OS, riziko úmrtí se snížilo o 25 % ve srovnání se samotnou platinou-etoposidem (HR = 0,75 [95% CI: 0,62–0,91], p = 0,0032). Po 12 měsících od zahájení léčby žil vyšší podíl pacientů léčených durvalumabem plus platinou-etoposidem ve srovnání se samotnou chemoterapií (52,8 vs. 39,3 %). Stejně tomu bylo po 18 měsících (32 vs. 24,8 %), resp. 24 měsících (22,2 vs. 14,4 %) (graf 4).
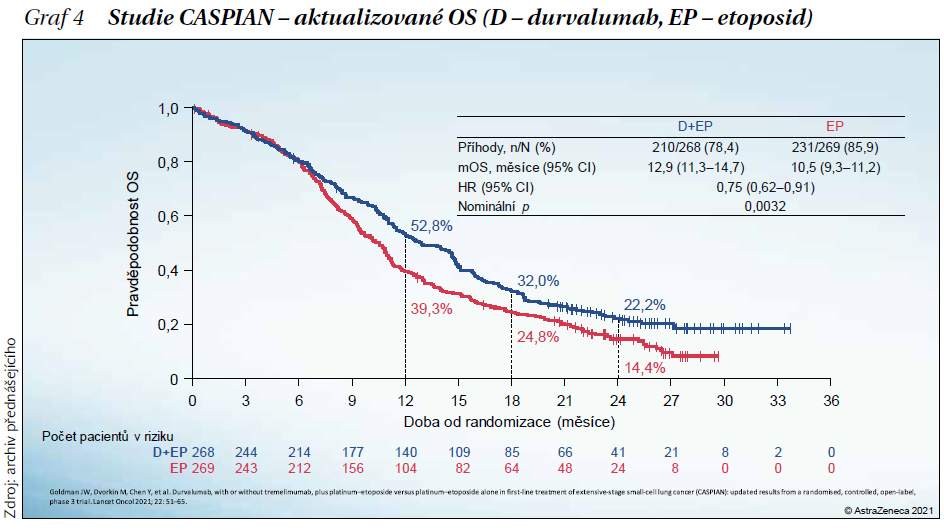
U obou skupin byla pozorována velmi nízká prevalence exprese PD-L1 na nádorových nebo imunitních buňkách. Počet pacientů bez progrese onemocnění léčených kombinací durvalumab plus platinaou-etoposidem (18 %, 95% CI: 13,1–22,5) v 1. roce byl ve srovnání s léčbou platinou-etoposidem (5 %, 95% CI: 2,4– 8,0) více než trojnásobný (graf 5).
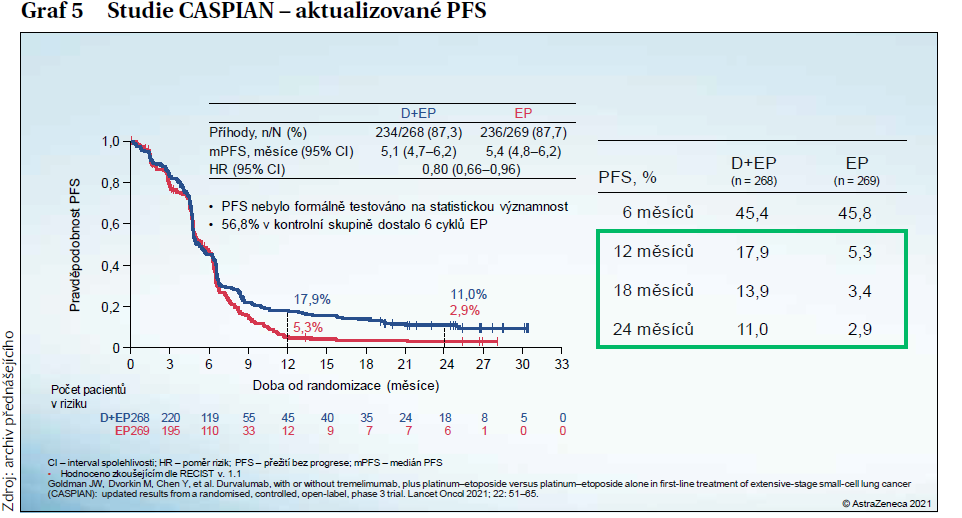
Závěry studie CASPIAN: Nedávno publikované aktualizované výsledky demonstrovaly, že nasazení kombinované léčby durvalumabem plus platinou-etoposidem vedlo k prodloužení celkové doby přežití při zachování kvality života. Tato léčba přinesla konzistentní zlepšení OS napříč všemi předem specifikovanými podskupinami. Mezi oběma skupinami nebyl pozorován žádný rozdíl v incidenci nových mozkových/CNS metastáz.
Kombinovaná léčba durvalumabem plus platinou-etoposidem je jediná schválená imunoterapie, která ve srovnání s léčbou samotnou platinou-etoposidem vykazuje zvýšení ORR u pacientů s ES-SCLC (67,9 vs. 58,0 %), ovšem medián délky trvání odpovědi DoR odpovídal v obou ramenech 5,1 měsíce. Při první progresi se nové léze vyskytly kvantitativně méně často u pacientů léčených durvalumabem plus platinou-etoposidem oproti kontrolní skupině. Nežádoucí účinky odpovídaly známým bezpečnostním profilům všech použitých léčivých přípravků. Četnost nežádoucích příhod stupně 3 nebo 4 byla v obou skupinách stejná. V rameni s durvalumabem se u 20 % pacientů vyskytly imunitně zprostředkované nežádoucí příhody, většinou stupně 1 nebo 2.
Závěr
Pro účinnou diagnostiku a následnou léčbu karcinomu plic je nezbytný důkladný staging, stanovení resekability a určení vhodného léčebného plánu pro danou formu onemocnění. Imunoterapie je dynamicky rozvíjející se oblastí systémové onkologické léčby s velkým potenciálem v léčbě pacientů s plicním karcinomem s dobrým bezpečnostním profilem. Výsledky studií PACIFIC a CASPIAN potvrzují efektivitu nasazení imunoterapie durvalumabu jako konsolidační léčby pacientů s lokálně pokročilým neoperovatelným NSCLC exprimujícím PD-L1 na ≥ 1 % nádorových buněk, u kterých nedošlo k progresi po CRT, jakož i u pacinetů s ES-SCLC v první linii. Studie ADAURA demonstrovala vysoce signifikantní účinky osimertinibu v adjuvantní léčbě po úplné resekci nádoru u pacientů s EGFRm NSCLC.
Alexandra Izraelová
