Přehledový článek se zabývá dvěma formami pokročilého karcinomu prostaty, jednak metastatického hormon senzitivního karcinomu prostaty, jednak nemetastatického kastračně rezistetního karcinomu prostaty. Jsou diskutovány možnosti terapie zaměřené hlavně na léčbu cílenou na androgenní receptor, kam řadíme významný antiadrogen 2. generace darolutamid. V obou formách onemocnění prokázal jednoznačný benefit na prodloužení celkového přežití pacientů. Důležitou skutečností je také výborná snášenlivost tohoto léku při dlouhodobě trvající léčbě.
Karcinom prostaty je nejčastěji maligní onemocnění u mužů (po vyčlenění nemelanomových nádorů kůže). Vzhledem k pomalému růstu karcinomu prostaty v počátečních fázích onemocnění a široce rozšířeným odběrům na prostatický specifický antigen (PSA) je onemocnění převážně diagnostikováno v lokalizovaném stadiu, které je omezené na prostatu. Nemocní jsou indikováni k lokální léčbě (radikální prostatektomii – RAPE – nebo radioterapii). U vybrané skupiny pacientů lze volit i možnost aktivního sledování či observace. I přes lokální terapii dochází u části pacientů postupně k elevaci PSA, která je častokrát spojena s nálezem vzdálených metastáz, hlavně v oblasti skeletu či lymfatických uzlin.
Metastatický karcinom prostaty může ale být také diagnostikován i primárně, mluvíme následně o de novo metastatickém onemocnění. Metastatický karcinom prostaty je zpočátku hormon senzitivní onemocnění. V literatuře se pro toto onemocnění užívá často zkratka mHSPC (metastatic hormon-sensitive prostate cancer). Základem léčby je androgen deprivační léčba (ADT). Účinnost primární ADT je většinou omezena na 2–3 roky. Postupně pak dochází k další elevaci PSA a radiologické progresi i přes trvající kastrační hodnoty testosteronu. Onemocnění se stává metastatickým kastračně rezistentním (metastatic castrate-resistant prostate cancer – mCRPC). Existuje ale skupina pacientů, u kterých elevuje PSA (při podávaní ADT) a současně podle zobrazovacích vyšetření (CT, scintigrafie skeletu, MRI, nebo PET/CT) nemají průkaz vzdálené diseminace. Toto onemocnění definujeme jako nemetastatický CRPC (nmCRPC), pro které nebyla donedávna k dispozici žádná účinná léčba.
V posledních letech proběhlo mnoho klinických studií s cílem zlepšit léčebné výsledky pokročilého karcinom prostaty. V případě mHSPC prokázala benefit u pacientů kombinace ADT + chemoterapie, ADT + ARTA (androgen receptor target therapy – léčba cílená na androgenní receptor) a nově i triplet (ADT + chemoterapie + ARTA). V případě nmCRPC se v při onemocnění s vyšším rizikem (čas zdvojení PSA pod 10 měsíců) uplatňuje kombinace ADT + ARTA.
Jedním z představitelů ARTA je darolutamid, který prokázal účinnost jak u pacientů s mHSPC, tak i v případě pacientů s nmCRPC.
Darolutamid
Darolutamid je představitel inhibitorů AR druhé generace. Na rozdíl od enzalutamidu a apalutamidu, je struktura darolutamidu více polární se zvýšeným potenciálem vytvářet vodíkové můstky. Má vyšší afinitu k AR než enzalutamid nebo apalutamid. Polární struktura je spojena s nižším průchodem přes hematoencefalickou bariéru s nižším výskytem nežádoucích účinků na centrální nervový systém. Darolutamid dále prokázal menší míru interakce se skupinou enzymů cytochromu P450, což lze s výhodou využít v praxi při současném podávaní léčiv, jako např. opiátů, antikoagulancií, inhibitorů protonové pumpy. Podávají se perorálně dvě 300mg tbl. 2× denně (celková dávka 1 200 mg denně). Léčba je dlouhodobá do objevení projevů závažné toxicity, do progrese onemocnění, či ukončení z jiných důvodů (například na žádost pacienta).
Darolutamid v léčbě mHSPC
Jak bylo zmíněno výše, základem léčby mHSPC je podání ADT. Kombinovaná léčba ale významně zlepšila léčebné výsledky tohoto onemocnění. Důležitou skutečností je klasifikace mHSPC podle rizika a rozsahu postižení.
Klinické studie hodnotící přínos kombinace ADT + docetaxel definovaly skupinu pacientů s takzvaným high-volume onemocněním. Toto onemocnění bylo definováno přítomností viscerálního postižení a/nebo přítomností čtyř a více metastatických lokalit ve skeletu, z toho jedno ložisko by mělo být mimo obratle a pánevní kosti. Právě tato skupina nemocných měla přínos z přidání docetaxelu.
Studie hodnotící kombinace ADT + abirateron definovaly high-risk onemocnění s přítomností alespoň dvou znaků: GS ≥ 8, tři a více kostních metastáz či přítomností viscerálních metastáz. Abirateron prokázal největší přínos u pacientů s de novo mHSPC a v případě vysokého rizika.
Další představitelé ARTA – apalutamid a enzalutamid – mají účinnost v celé populaci mHSPC, bez ohledu na riziko. Nutno zmínit, že skupina pacientů s high-volume onemocněním není totožná se skupinou s high-risk onemocněním, kdy může dojít až téměř ke 20% rozdílu.
Další možností, jak ještě případně zlepšit léčebné výsledky u pacientů s mHSPC je triplet ADT + docetaxel + ARTA. V této kombinaci byl prokázán účinek abirateronu, nicméně nejsilnější data máme v případě kombimace ADT + docetaxel + darolutamid.
Kombinaci hodnotila klinická studie III. fáze ARASENS. Studie hodnotila celkem 1 306 pacientů s mHSPC bez předchozí léčby. ADT mohla být zahájena nejvíce 12 týdnů před randomizací. Pacienti byli randomizováni v poměrů 1 : 1 ADT + docetaxel + darolutamid vs. ADT + docetaxel + placebo. Primárním cílem studie bylo zhodnocení OS. Docetaxel byl aplikován celkem v šesti cyklech, dávka 75 mg/m2 à 3 týdny. Darolutamid byl podáván v dávce 600 mg 2× denně. Ve studii dominovali pacienti s de novo metastatickým onemocněním (86,1 %). Klinická studie prokázala významné prodloužení mediánu celkového přežití (mOS) (HR 0,68, 95% CI 0,57–0,80) s 32,5 % redukcí rizika úmrtí (graf 1).
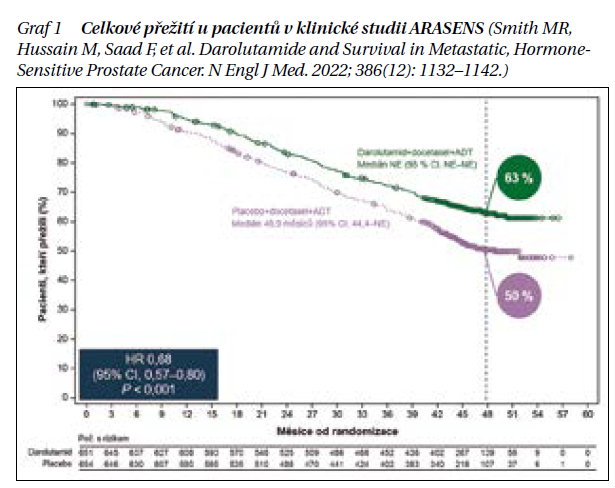
Efekt na prodloužení OS přetrvával i přes další účinnou léčbu u pacientů v kontrolním ramenu. Podobně bylo významné prodloužení i další cíle studie: čas do vzniku mCRPC, čas do objevení se bolestí, čas do objevení se závažné události či času do zahájení další linie onkologické léčby (tabulka 1).
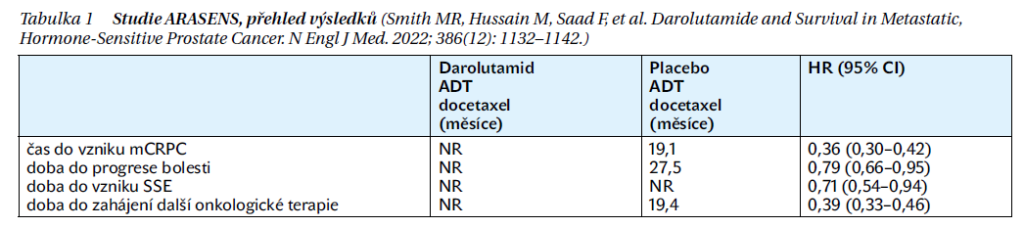
Důležitou skutečností klinické studie ARASENS byla dobrá snášenlivost trojkombinace. Toxicita stupně 3 a 4 byla v obou skupinách pacientů podobná (44,8 vs. 42,3 %). Mezi nejčastěji reportované projevy toxicity trojkombinace patřily neutropenie, arteriální hypertenze, anémie, pneumonitida. Důležitým ukazovatelem účinnosti tripletu je časný pokles PSA pod možnosti detekce.
V post hoc analýze studie ARASENS prokázala skupina pacientů s poklesem PSA pod detekovatelnou hladinu 24 týdnů od zahájení léčby výrazné prodloužení OS ve srovnání se skupinou, kde tento pokles nebyl zaznamenán (HR 0,47, 95% CI 0,35–0,63).
V době zahájení klinické studie ARASENS ještě nebyly známy finální výsledky klinických studií LATITUDE a CHAARTED, které hodnotily u pacientů s mHSPC význam kombinace ADT + abirateron a ADT + docetaxel. Zmíněné klinické studie stratifikovaly pacienty na již výše uvedené skupiny podle rizika, či podle objemového postižení. Studie ARASENS proto primárně stratifikaci na tyto skupiny nedefinovala, ale proběhla post hoc analýza, kde již retrospektivně byli pacienti klasifikováni do jednotlivých skupin. Jednoznačný přínos tripletu ADT + darolutamid + docetaxel na prodloužení OS byl prokázán u nemocných s vysokým rizikem (HR 0,71, 95% CI 0,58–0,86), vysokým objemovým postižením (HR 0,69, 95% 0,57–0,82) a také ve skupině s nižším rizikem (HR 0,62, 95% CI 0,42–0,90). Trend byl zaznamenán u nemocných s menším objemovým postižením (HR 0,68, 95% CI 0,41–1,13), což mohlo být způsobeno také nižším počtem sledovaných pacientů. Doba do vzniku metastatického CRPC byla jednoznačně delší ve všech podskupinách pacientů léčených tripletem ve srovnání s dubletem ADT + docetaxel.
Triplet ADT + docetaxel + darolutamid představuje novou léčebnou možnost u pacientů s mHSPC. Jednozančně byl prokázán přínos ve srovnání s kombinací ADT + docetaxel. Proto hlavně u pacientů s rozsáhlejším onemocněním, s klinickými projevy, kde uvažujeme o podání chemoterapie, bychom měli zvážit i možnost tripletu, který je podle všech důkazů účinnější. Důležitou skutečností je také srovnatelná toxicita obou léčebných kombinací.
Darolutamid v léčbě nmCRPC
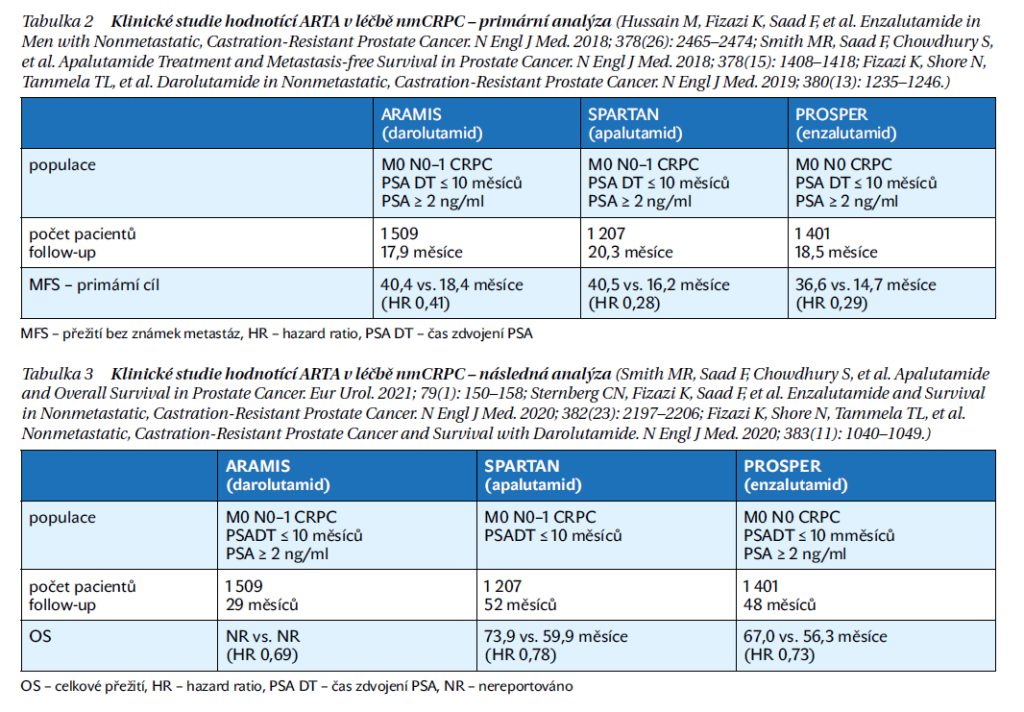
Nemocní s nmCRPC jsou převážně bez klinických potíží, bez symptomatologického onemocnění. U většiny pacientů s nmCRPC ale dochází k rozvoji kostních či uzlinových metastáz, bez terapie v průběhu 1–3 let. Vznik metastáz, hlavně kostních, je spojen s možnými komplikacemi, jako jsou bolesti, patologické fraktury, zhoršení celkového výkonnostního stavu apod. Proto jedním z cílů léčby nmCRPC je prodloužit dobu do vzniku metastatického onemocnění. Až donedávna nebyla k dispozici žádná účinná léčba tohoto onemocnění. Podle konvenčního zobrazení pomocí CT vyšetření či scintigrafie skeletu je ale průkaz metastáz vzácný při hodnotách PSA pod 10 ng/ml. Kromě vlastní hodnoty PSA je ale důležitým faktorem i rychlost vzestupu koncentrace PSA. U pacientů s časem zdvojení PSA (PSA doubling time – PSA DT) pod 8–10 měsíců významně stoupá riziko vzniku metastáz. Právě tato riziková skupina nemocných je ohrožena časným vznikem metastatického onemocnění. Možnosti, jak zlepšit léčebné výsledky této skupiny, je přidat ARTA k ADT. Proběhly 3 významné klinické studie fáze III, které hodnotily postavení ARTA v léčbě nmCRPC – apalutamid – studie SPARTAN, darolutamid – studie ARAMIS a enzalutamid – studie PROSPER. Všechny 3 studie zásadně prokázaly prodloužení času do vzniku metastatického onemocnění při výborné toleranci léčby ARTA ve srovnání s placebem a v následných analýzách i významné prodloužení celkového přežití. Do studie byli zařazeni rizikoví pacienti s časem zdvojení PSA ≤ 10 měsíců a hodnotou PSA 2 ng/ml a více. Přehled výsledků zmíněných klinických studií je uveden v tabulkách 2 a 3.
Toxicita, lékové interakce
Jak je vidět s léčebných výsledků, jedná se o dlouhodobou terapii. Proto je důležitou součástí léčby i přijatelná toxicita. Všechny preparáty potvrdily tuto skutečnost, v onkologii se jedná o jeden z nejlépe tolerovatelných typů léčby. I přes podobné výsledky se ale jednotlivé preparáty liší. Darolutamid ve srovnání s enzalutamidem a apalutamidem má strukturu více polární se zvýšeným potenciálem vytvářet vodíkové můstky. Má vyšší afinitu k androgennímu receptoru než enzalutamid nebo apalutamid. Polární struktura je spojena s nižším průchodem přes hematoencefalickou bariéru s nižším výskytem nežádoucích účinků na centrální nervový systém. Toto lze s výhodou využít u pacientů s onemocněním mozku v anamnéze. Darolutamid dále prokázal menší míru interakce se skupinou enzymů cytochromu P450, což se dá s výhodou využít v praxi při současném podávaní léčiv, jako např. opiátů, antikoagulancií, inhibitorů protonové pumpy. Zdá se, že darolutamid má nejvíce přijatelnou snášenlivost léčby. Nejčastějším projevem toxicity byla únava.
Závěr
Podání ARTA jednoznačně zlepšilo léčebné výsledky pacientů s nmCRPC s časem zdvojení PSA pod 10 měsíců. Při výpočtu tohoto ukazatele lze využít on-line kalkulátory (např. MSKCC), které dovolují predikovat čas zdvojení PSA již pomocí 2–3 odběrů v rozmezí 2–3 týdnů a umožní zahájení terapie mnohem dříve než čekat 10 měsíců na „reálný“ průběh koncentrace PSA. Podmínkou je obecná definice CRPC, tedy vstupní hodnota PSA by měla být ≥ 2 ng/ml.
doc. MUDr. Igor Richter, Ph.D.1,2,3
doc. MUDr. Josef Dvořák, Ph.D.2
MUDr. Sofya Al-Samsan 1
MUDr. Jiří Bartoš, MBA1
1 Onkologické oddělení, Krajská nemocnice Liberec
2 Onkologická klinika 1. LF UK a Fakultní Thomayerovy nemocnice, Praha
3 Fakulta zdravotnických studií, Technická univerzita Liberec
